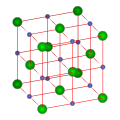
Natria klorido
| Natria klorido | |||||||
|---|---|---|---|---|---|---|---|
| Struktura formulo | |||||||

| |||||||
| speco de kemia ento | |||||||
| salo • klorido | |||||||
| __ Na+ __ Cl− | |||||||
| kristala sistemo | kuba | ||||||
| kristala spacgrupo | |||||||
| strukturaj parametroj | a = 562 pm[1] | ||||||
| Koordinaj nombroj | Na[6], Cl[6] | ||||||
| Ĝeneralaĵoj | |||||||
| Nomo | Natria klorido | ||||||
| Kemia formulo | NaCl | ||||||
| CAS-numero-kodo | 7647-14-5 | ||||||
| PubChem-kodo | 5234 | ||||||
| ChemSpider-kodo | |||||||
| Konciza priskribo | senkolora kaj senodora solidaĵo[2] | ||||||
| Karakterizaĵoj | |||||||
| Fazo de materio | solida | ||||||
| Denseco |
2,17 g·cm−3 (20 °C)[2] | ||||||
| Frostopunkto | |||||||
| Fandopunkto |
801 °C (1,474 °F; 1,074 K) | ||||||
| Bolpunkto | |||||||
| Solvebleco | bona en akvo (359 g·l−1 je 20 °C[3]) | ||||||
| Refrakta indico | 1,5442 ĝis 1,5589 [4] | ||||||
| Sekurecaj indikoj | |||||||
| |||||||
| Mortiga dozo (LD50) |
3000–8000 mg/kg (buŝe, muso) | ||||||
| Se eble, uziĝu unuoj de la Sistemo Internacia de Unuoj. Escepte de la notoj alie indikitaj, la datumoj rilatas al materialoj laŭ la ordinaraj normoj pri temperaturo kaj premo (25o kaj premo je 1 atmosfero aŭ 760 mm de Hg). | |||||||
|
Termodinamike | |
|---|---|
| ΔfH0g | -181.42 kJ/mol |
| ΔfH0l | -385.92 kJ/molo |
| ΔfH0s | -411.12 kJ/mol |
| S0g, 1 baro | 229.79 J/molo·K |
| S0l, 1 baro | 95.06 J/molo·K |
| S0s | 72.11 J/molo·K |
|
Danĝero | |
| Enpreno | dangera en grandaj kvantoj |
| Enspiro | povas inciti |
| Haŭto | povas inciti |
| Okuloj | povas inciti |
| Pliaj informoj en la angla | Hazardous Chemical Database |
|
SI-unuoj estis uzataj laŭeble.
| |
Natria klorido (ankaŭ konata kiel tabla salo aŭ kuirsalo) estas la plej ofte uzata salo, spico ofte uzata en kuirarto por bongustigi aŭ konservi manĝaĵojn.
Ne estas bone por la sano, manĝi tro da natrio, ĉar tiel via sango-premo povas tro altiĝi. Vi povas anstataŭ manĝi multe da salo natria, manĝi version kiu enhavas Kalion anstataŭ natrion sed kiu gustas simile ĉar ĝi ankoraŭ havas kloridon. Vi rajtas manĝi 6 gramojn de natrio en ĉiu tago, sed multaj prenas pli ĉar ekzistas grandkvante en manĝaĵoj jam pretigitaj. Por eviti tiel manĝi multe da salo, estas plej simple kuiri mem, tiel vi povas regi ĉu vi enmetas salon.
Referencoj
- ↑ M. Straumanis, A. Ievins: Die Gitterkonstanten des NaCl und des Steinsalzes, Zeitschrift für Physik, 1936, 102, S. 353–359.
- ↑ 2,0 2,1 2,2 2,3 Enskribo al Natriumchlorid en la GESTIS-substanca datenbanko de la IFA, vokita la 29-an de aprilo 2013 (JavaScript necesa).
- ↑ CRC Handbook of Chemistry and Physics, 88th edition, 2008.
- ↑ http://refractiveindex.info/?group=CRYSTALS&material=NaCl