Butila izocianido
| n-Butila izocianido | |||
Butila izocianido | |||
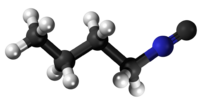 | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 2769-64-4 | ||
| ChemSpider kodo | 68507 | ||
| PubChem-kodo | 76008 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ flava likvaĵo | ||
| Molmaso | 83,134g mol−1 | ||
| Denseco | 0,795g/cm−3[1] | ||
| Bolpunkto | 117 °C | ||
| Refrakta indico | 1,396 | ||
| Acideco (pKa) | 16,22 | ||
| Ekflama temperaturo | 20,5 °C [2] | ||
| Solvebleco | Akvo:5 g/L | ||
| Mortiga dozo (LD50) | 360 mg/kg (buŝe) [3] | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H302, H312, H332 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P280, P301+312, P302+352, P303+361+353, P304+312, P304+340, P312, P330, P363, P370+378, P403+235, P501 | ||
(25 °C kaj 100 kPa) | |||
n-Butila izocianido estas kemia komponaĵo kun molekula formulo C4H9-N≡C estas izomero de la n-butila cianido aŭ
C4H9-C≡N. Saloj kaj esteroj de la izocianida acido nomatas izocianidoj. Butila izocianido estas senkolora likvaĵo, danĝera kaj toksa substanco kun malaltaj fandopunkto kaj bolpunkto. Kiel ĉiuj izocianidoj, ĝi estas malagrablodora kaj ne solvebla en akvo, sed solvebla en alkoholo kaj etero.
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Preparado de n-butila izocianido per senhidratigo de la n-butila formamido:
Reakcio 2[redakti | redakti fonton]
- Preparado de n-butila izocianido per interagado de n-butila formamido kun fosfora pentoksido:
Reakcio 3[redakti | redakti fonton]
- Preparado de n-butila izocianido per interagado de n-butila formamido kun tionila klorido:
Reakcio 4[redakti | redakti fonton]
- Preparado de n-butila izocianido per interagado de n-butila klorido kun arĝenta (I) izocianido:[4]
Reakcio 5[redakti | redakti fonton]
- Preparado de n-butila izocianido per alkohola transesterigo inter propila izocianido kun n-butila alkoholo:
Reakcio 6[redakti | redakti fonton]
- Preparado de n-butila izonitrilo per traktado de n-butilamino kun kloroformo en ĉeesto de kalia hidroksido:
Reakcio 7[redakti | redakti fonton]
- Per hidrolizo n-butila isocianido produktas n-butilaminon kaj formiata acidon:[5]





![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)







