Izobutila acetato
| Izobutila acetato | |||
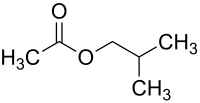 | |||
| Plata kemia strukturo de la Izobutila acetato | |||
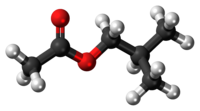 | |||
| Tridimensia kemia strukturo de la Izobutila acetato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 110-19-0 | ||
| ChemSpider kodo | 7747 | ||
| PubChem-kodo | 8038 | ||
| Merck Index | 15,5175 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora, brulema likvaĵo kun agrabla odoro | ||
| Molmaso | 116,16 g·mol−1 | ||
| Denseco | 0,875g cm−3 | ||
| Fandpunkto | −99 °C[1] | ||
| Bolpunkto | 118 °C | ||
| Refrakta indico | 1,3902[2] | ||
| Ekflama temperaturo | 22 °C[3] | ||
| Memsparka temperaturo | 510 °C[3] | ||
| Solvebleco | Akvo:6,3 g/L | ||
| Mortiga dozo (LD50) | 1763 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R11 R66 | ||
| Sekureco | S16 S23 S25 S29 S33 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H336 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P271, P280, P303+361+353, P304+340, P370+378, P403+233, P403+235, P405, P501][4] | ||
(25 °C kaj 100 kPa) | |||
Izobutila acetato aŭ C6H12O2 estas kemia kombinaĵo, apartenanta al la funkcia grupo de la esteroj de la acetata acido kaj izobutanolo, senkolora, brulema likvaĵo kun agrabla odoro, uzata kiel solvanto kaj kiel gustiga kaj odorigagento. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Izobutila acetato estas malmulte solvebla en akvo, sed estas tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj.
Izobutila acetato ankaŭ uzatas kiel solvanto por farboj. Ĝi reakcias kun acidoj kaj alkoholoj liberigante grandan kvanton da energio kaj varmo. Fortaj oksidigaj acidoj povas kaŭzi eksplodan reakcion sufiĉe alta por ekbruli la produktojn de la reakcio. Granda amaso da varmo ankaŭ liberiĝas per interagado de la estero kun kaŭstikaj solvaĵoj. Kun alkalaj metaloj kaj alkalaj metaloj ĝi generas bruleman hidrogenon.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado per traktado de acetata acido kaj izobutanolo:
Sintezo 2[redakti | redakti fonton]
- Preparado per traktado de acetata anhidrido kaj izobutanolo:
Sintezo 3[redakti | redakti fonton]
- Preparado per traktado de izobutila klorido kaj acetata acido:
Sintezo 4[redakti | redakti fonton]
- Preparado per interagado de natria acetato kaj izobutila klorido:
Sintezo 5[redakti | redakti fonton]
- Reakcio de transesterigo inter izobutila formiato kaj metila acetato:
Sintezo 6[redakti | redakti fonton]
- Per transigo de la izobutila radikalo inter izobutila benzoato kaj acetata acido:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Hidrolizo de la izobutila acetato:
Reakcio 2[redakti | redakti fonton]
- Sapigo de la izobutila acetato:
Reakcio 3[redakti | redakti fonton]
- Reduktigo de la izobutila acetato:
Reakcio 4[redakti | redakti fonton]
- Per transesteriga reakcio inter izobutila acetato kaj anizila cinamato:
Reakcio 5[redakti | redakti fonton]
- Reakcio kun klorida acido:
Reakcio 6[redakti | redakti fonton]
- Reakcio kun amoniako:
Literaturo[redakti | redakti fonton]
- The Good Scents Company
- Butyl Acetates
- Patty's Toxicology
- Handbook of Environmental Fate and Exposure Data For Organic Chemicals
- A Comprehensive Guide to the Hazardous Properties of Chemical Substances
- Flavours and Fragrances: Chemistry, Bioprocessing and Sustainability
- Organic Chemistry, Volume One: Part I: Aliphatic Compounds







![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)

