Jodoacetata acido
| Jodoacetata acido | |||

| |||
| Kemia strukturo de la Jodoacetata acido | |||
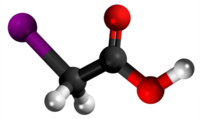
| |||
| 3D Kemia strukturo de la Jodoacetata acido | |||
| Kemia formulo | |||
| CAS-numero-kodo | 64-69-7 | ||
| ChemSpider kodo | 5050 | ||
| PubChem-kodo | 5240 | ||
| Fizikaj proprecoj | |||
| Molmaso | 185.95 g mol−1 | ||
| Smiles | C(C(=O)O)I | ||
| Fandopunkto | 81 °C (178 ℉; 354 K) | ||
| Bolpunkto | 208 °C (406 ℉; 481 K) | ||
| Solvebleco | Akvo:600 g/l | ||
| Merck Index |
| ||
| Sekurecaj Indikoj | |||
| Risko | R25 R35 | ||
| Sekureco | (S1/2) S22 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H301, H314 | ||
| GHS Deklaroj pri antaŭgardoj | P280, P301+310, P305+351+338, P310 | ||
Jodoacetata acido, hidrogena jodoacetato aŭ IH2C-COOH estas organika komponaĵo derivaĵo el acetata acido, toksa kaj koroda substanco, kaj tiel kiel multaj alkialaj halogenidoj, ĝi estas alkiligagento. Ĝi reakcias kun cisteino en proteinoj. Ĝi ofte uzatas kiel modifanto de la SH-grupo de la proteinoj por preventi la formigon de dusulfidaj ligoj post reduktiĝo de la reziduaj cisteinoj al cisteino dum la proteina sekvencado.
Jodoacetata acido estas teratogena agento kaj eĉ en etaj kvantoj ĝi povas okazigi damaĝojn al mambestaj ĉeloj. Jodoacetata acido same montriĝis tumorogena en musoj.[1] Fluoroacetata, kloroacetata, bromoacetata kaj jodoacetata acidoj estas pli fortaj ol acetata acido.
Sintezo[redakti | redakti fonton]
- Jodoacetata acido prepareblas per traktado de kloroacetata acido kaj kalia jodido:[2]
Reakcioj[redakti | redakti fonton]

La jodoacetata acido ofte uzatas kiel alkiligagento por protektado de reziduaj aminoacidoj de cisteino kiuj formiĝas. La reakcio estas konata kiel karbokso-metiligo kaj ĝi estas kovalenta, do neinversigebla.
En interagado de la jodoacetata acido kaj benzila alkoholo en ĉeesto de sulfata acido rezultas la estero benzila jodoacetato.
Proprecoj[redakti | redakti fonton]
Jodida jono nature okazas kaj troveblas en multaj naturaj akvofontoj kaj facile oksidiĝas per malinfektiloj de reziduaj akvoj. Unu el la produktoj de la jodida oksidigo estas la hipojodita acido kiu kapablas reakcii kun aliaj organikaj materialoj por generi jodohavajn desinfektajn kromproduktojn, inkluzive de jodoacetata acido. En studo farita de Plewa kaj aliaj kunuloj, la jodoacetata acido estis konsiderita unu el la plej citotoksaj el aliaj studitaĵoj, kies mortiga dozo estas proksimume 10−5.
Ĝi estas la plej genotoksa inter 60 aliaj flankproduktoj studitaj ĝis nun. Krom tio, jodoacetata acido estas pli teratogena ol ĝiaj analogoj same kiel bromoacetata acido kaj kloroacetata acido. Ĝia tokseco kunrilatas al ĝia kapableco kiel alkiligagento, en kiu ĝi modifas la cisteinajn reziduojn en proteinoj. Unuhalogenidaj acetataj acidoj estas la plej toksaj, kaj ĝia tokseco pligrandiĝas kun la grando de la halogenido.
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- SCBT
- ACS Publications
- Chemical Book
- Ionsource
- Haschek and Rousseaŭ's Handbook of Toxicologic Pathology, Wanda M. Haschek,Colin G. Rousseaŭ,Matthew A. Wallig
Halogenidaj derivaĵoj de acetata acido[redakti | redakti fonton]
-
Unujodoacetata acido
Referencoj[redakti | redakti fonton]
- ↑ Disinfection By-products in Drinking Water, K. Clive Thompson, Simon Gillespie, Emma H. Goslan
- ↑ Radiopharmacy, Manuel Tubis, Walter Wolf
- ↑ Cisteino peptidazo aŭ cisteino proteazo estas enzimo kiu degradigas proteinojn.