Metano-sulfonata anhidrido
| Metano-sulfonata anhidrido | |||
 | |||
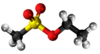
| Plata kemia strukturo de la Metano-sulfonata anhidrido | |||
 | |||
| Tridimensia kemia strukturo de la Metano-sulfonata anhidrido | |||
| Kemia formulo | |||
| CAS-numero-kodo | 7143-01-3 | ||
| ChemSpider kodo | 73591 | ||
| PubChem-kodo | 81560 | ||
| Alternativa(j) nomo(j) | |||
| |||
| Fizikaj proprecoj | |||
| Aspekto | blanka, koroda, higroskopa solidaĵo | ||
| Molmaso | 174,185 g·mol−1 | ||
| Denseco | 1,36g cm−3[1] | ||
| Fandpunkto | 69,5 °C | ||
| Bolpunkto | 105 °C[2] | ||
| Refrakta indico | 1,5365 | ||
| Solvebleco | Akvo:reakcias | ||
| Mortiga dozo (LD50) | 200 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R14 R35 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H314 | ||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P405, P501[3] | ||
(25 °C kaj 100 kPa) | |||
Metano-sulfonata anhidrido, mezilata acido aŭ C2H6O5S2 estas organika anhidrido de la metano-sulfonata acido, blanka, koroda kaj higroskopa solidaĵo, komerce disponebla kun 97%-98% da pureco kaj uzata kiel organika reakcianto en kemiaj sintezoj. Ĝi reakcias kun akvo per hidrolizo kaj estas solvebla en plejmulto el la senprotonaj organikaj solvantoj.
Metano-sulfonata anhidrido posedas unu metilan grupon (-CH3) ligitan al sulfonata grupo (-SO2OH). Sulfonata acido posedas unu sulfuratomon ligitan al unu karbonatomo el hidrokarbonido kaj ligita ankaŭ al tri oksigenatomoj, unu el kiuj estas aneksita al unu hidrogenatomo. Sulfonata acido havas acidajn proprecojn pro la hidrogenatomo, kaj ĝi estas pli forta acido ol karboksilataj acidoj. Metano-sulfonata anhidrido estas unu el la plej gravaj organosulfuraj komponaĵoj uzataj en organikaj sintezoj. Ĝi uzatas kiel katalizitlo en esterigoj, alkiligoj kaj kondensigaj reakcioj. Metano-sulfonatoj estas saloj kaj esteroj de la metano-sulfonata acido.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado per senhidratigo kun fosfora kvinoksido kaj metano-sulfonata acido:
Sintezo 2[redakti | redakti fonton]
- Per senhidratigo de la metano-sulfonata acido en ĉeesto de sulfata acido:
Sintezo 3[redakti | redakti fonton]
- Per traktado de metano-sulfonata acido kun sulfura trioksido donante metano-sulfonatan anhidridon kaj sulfatan acidon:[4]
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- * Primaraj kaj sekundaraj alkoholoj povas oksidiĝi al aldehidoj kaj ketonoj kun bona rendimento uzante metanosulfonata anhidrido. Benzila alkoholo povas konvertiĝi al benzaldehido per ĉi-metodo:[5]
Reakcio 2[redakti | redakti fonton]
- Esterigo de la metano-sulfonata anhidrido kun etanolo en acida medio:
Reakcio 3[redakti | redakti fonton]
- Preparado de klorido de metano-sulfonilo per interagado de la metano-sulfonata anhidrido kun klorida acido:
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- Reag.paperplane Arkivigite je 2018-11-20 per la retarkivo Wayback Machine
- Pharmaceutical Process Chemistry for Synthesis
- Heterocycles Synthesis With Eaton's Reagent
- Essentials of Organic Chemistry: For Students of Pharmacy, Medicinal Chemistry and Biological Chemistry
- Sulfur-Containing Reagents
- Chemicalland21
Referencoj[redakti | redakti fonton]
- ↑ Chemical Book
- ↑ Merck Millipore. Arkivita el la originalo je 2018-11-21. Alirita 2018-11-20.
- ↑ Pubchem
- ↑ Mechanistic aspects in aromatic sulfonation and desulfonation
- ↑ Sulfur-Containing Reagents





![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{0^{o}C}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/658488f90e6a9fa0944b860221639e523bbab13d)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{H_{2}SO_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f9dc5b9288971b463560cad8050dd6ff7c06f487)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)
![{\displaystyle {\mathsf {{\xrightarrow[{Acetata\,acido}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/82a3a54a5bef6a938983b90538fca9ff25898680)