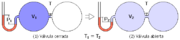Leĝo de Boyle: Malsamoj inter versioj
| [nekontrolita versio] | [nekontrolita versio] |
Enhavo forigita Enhavo aldonita
e roboto aldono de: fr:Loi de Boyle-Mariotte |
Neniu resumo de redakto |
||
| Linio 1: | Linio 1: | ||
La '''leĝo de Boyle''' diras, ke |
La '''leĝo de Boyle-Mariotte''' (aŭ leĝo de Boyle) diras, ke |
||
: la volumeno de certa [[maso]] da [[gaso]] je konstanta temperaturo estas inverse proporcia al sia [[premo]]. |
: la volumeno de certa [[maso]] da [[gaso]] je konstanta temperaturo estas inverse proporcia al sia [[premo]]. |
||
Ekzemple, se la premo de unu gaso duobliĝas, la volumeno de la gaso reduktiĝos duone, kaj same inverse. La leĝon ektrovis en [[1662]] la [[Irlando|irlanda]] [[Fiziko|fizikisto]] kaj [[Kemio|ĥemiisto]] [[Robert Boyle]]. |
Ekzemple, se la premo de unu gaso duobliĝas, la volumeno de la gaso reduktiĝos duone, kaj same inverse. La leĝon ektrovis en [[1662]] la [[Irlando|irlanda]] [[Fiziko|fizikisto]] kaj [[Kemio|ĥemiisto]] [[Robert Boyle]]. |
||
Kiel registrite je 20:40, 1 okt. 2010
La leĝo de Boyle-Mariotte (aŭ leĝo de Boyle) diras, ke
Ekzemple, se la premo de unu gaso duobliĝas, la volumeno de la gaso reduktiĝos duone, kaj same inverse. La leĝon ektrovis en 1662 la irlanda fizikisto kaj ĥemiisto Robert Boyle.
Eksteraj ligiloj
greke http://www.thescubaguide.com/certification/boyles-law.aspx greke http://dbhs.wvusd.k12.ca.us/webdocs/GasLaw/Gas-Boyle-Data.html