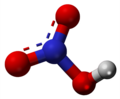
Arĝenta (I) hidroksido
Aspekto
| Arĝenta hidroksido | ||
| Kemia formulo | ||
 | ||
| Alternativa(j) nomo(j) | ||
| ||
| CAS-numero-kodo | 12673-77-7 12258-15-0 | |
| ChemSpider kodo | 8305469 | |
| PubChem-kodo | 10129950 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka solidaĵo | |
| Molmaso | 124,875g mol−1[1] | |
| Acideco (pKa) | 3,96 | |
| Solvebleco | Akvo:Nesolvebla | |
| Mortiga dozo (LD50) | >2000 mg/kg (buŝe) | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P264, P264+265, P280, P302+352, P305+354+338, P317, P321, P332+317, P362+364 | |
(25 °C kaj 100 kPa) | ||
Arĝenta hidroksido aŭ hidroksido de arĝento (I) estas neorganika kunmetaĵo apartenanta al la familio de la hidroksidoj. Ĝi estiĝas per hidratigado de la aluminia oksido kaj estas unu el la gravaj kombinaĵoj de la aluminio. Ĝi ordinare aperas kiel blankaj kristaloj kiuj malheliĝas spontanee pro formado de la arĝenta (I) oksido.
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Preparado de arĝenta hidroksido per hidrolizo de la arĝenta oksido:
Reakcio 2
[redakti | redakti fonton]- Preparado de arĝenta hidroksido per hidratigado de la kemia elemento arĝento:
Reakcio 3
[redakti | redakti fonton]- Preparado de arĝenta hidroksido per hidrolizo de la arĝenta sulfato:
Reakcio 4
[redakti | redakti fonton]- Preparado de arĝenta oksido per senhidratigado de arĝenta hidroksido:
Reakcio 5
[redakti | redakti fonton]- Reakcio de arĝenta hidroksido kun klorida acido donante arĝentan (I) kloridon
Reakcio 6
[redakti | redakti fonton]- Reakcio de arĝenta (I) hidroksido kun nitrata acido donante arĝentan (I) nitraton




![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)


![{\displaystyle {\mathsf {{\xrightarrow[{}]{varmo}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/39f1c6c7ab29f583de5842596076f1dac2b5b61a)