Ora (III) hidroksido
Aspekto
| Ora (III) hidroksido | ||
| Kemia formulo | ||
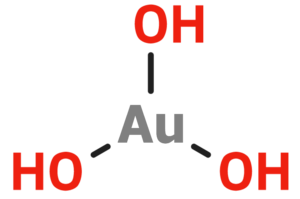 | ||
Ora (III) hidroksido | ||
 | ||
 | ||
| Flavaj kristaloj de ora (III) hidroksido. | ||
| Alternativa(j) nomo(j) | ||
| ||
| CAS-numero-kodo | 1303-52-2 54182-83-1 | |
| ChemSpider kodo | 19975363 | |
| PubChem-kodo | 102103 | |
| Fizikaj proprecoj | ||
| Aspekto | Vivantaj, malhelhelflavaj, lumsensivaj kristaloj[1] | |
| Molmaso | 247,991g mol−1 | |
| Fandpunkto | 305°C | |
| Bolpunkto | 698°C [2] | |
| Solvebleco | Akvo:0,0769 g/L Ruĝa ora hidroksido: Kps 2.5× 10-8 Blanka ora hidroksido: Kps 2.5× 10-5[3] | |
| Mortiga dozo (LD50) | 75 mg/kg (buŝe) | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P264+265, P271, P280, P302+352, P304+340, P305+351+338, P319, P321, P332+317, P337+317, P362+364, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Ora (III) hidroksido aŭ hidroksido de oro (III) estas neorganika kombinaĵo apartenanta al la familio de la hidroksidoj, rezultanta el hidratagado de la ora oksido aŭ hidrolizo de oraj saloj kaj esteroj. Ora (III) hidroksido estas vivantaj, malhelhelflavaj, lumsensivaj kristaloj, nesolveblaj en akvo kaj uzatas en kemiaj sintezoj. Ora (III) hidroksido prezentas tri hidroksilajn grupojn ligitan al oratomo. Ĝi konsistas je 1 oratomo, 3 hidrogenatomoj kaj 3 oksigenatomoj ĉiuj interkonektitaj per jonaj ligaĵoj. Ora hidroksido malkomponiĝas tiam kiam ekspoziciata al lumo. Ĝi estas neakordigebla kun fortaj oksidigagentoj. Oraj kombinaĵoj estas forte toksaj pro iliaj ekstremaj oksidigaj potencoj.
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Preparado de ora hidroksido per hidrolizo de la ora oksido:
Reakcio 2
[redakti | redakti fonton]- Preparado de ora hidroksido per traktado de ora nitrato kun natria hidroksido:
Reakcio 3
[redakti | redakti fonton]- Preparado de ora hidroksido per hidrolizo de la ora sulfato:
Reakcio 4
[redakti | redakti fonton]- Preparado de ora oksido per senhidratigado de ora hidroksido:
Reakcio 5
[redakti | redakti fonton]- Reakcio de ora hidroksido kun klorida acido donante oran trikloridon:
Reakcio 6
[redakti | redakti fonton]- Preparado de ora (III) hidroksido per traktado de ora (III) klorido kun kalia karbonato:
Reakcio 7
[redakti | redakti fonton]- Reakcio de ora (III) hidroksido kun bromo donante oran (III) oksidon:
Reakcio 8
[redakti | redakti fonton]- Preparado de kalia tetrakloroaŭrato (III) per traktado de ora (III) klorido kun kalia klorido:



![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)








![{\displaystyle {\mathsf {{\xrightarrow[{}]{varmo}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/39f1c6c7ab29f583de5842596076f1dac2b5b61a)