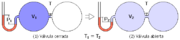Leĝo de Boyle: Malsamoj inter versioj
| [nekontrolita versio] | [nekontrolita versio] |
Enhavo forigita Enhavo aldonita
KuBOT (diskuto | kontribuoj) e Roboto: anstataŭigo de "Ŝablono:El" per "Ŝablono:EL" (laŭ VP:AA); kosmetikaj ŝanĝoj |
KuBOT (diskuto | kontribuoj) e Anstataŭigo de ne plu uzota Ŝablono:EL; vidu VP:DT en Marto 2017 |
||
| Linio 7: | Linio 7: | ||
== Eksteraj ligiloj == |
== Eksteraj ligiloj == |
||
* http://www.thescubaguide.com/certification/boyles-law.aspx <!-- en:Boyle's Law en->eo:_Boyle_'s (Juro, Leĝo) --> |
|||
* http://dbhs.wvusd.k12.ca.us/webdocs/GasLaw/Gas-Boyle-Data.html |
|||
[[Dosiero:Ley de Boyle Mariotte.png|thumb|left|180px]] |
[[Dosiero:Ley de Boyle Mariotte.png|thumb|left|180px]] |
||
[[Dosiero:Legge di Boyle dati originali.jpg|thumb|left|180px]] |
[[Dosiero:Legge di Boyle dati originali.jpg|thumb|left|180px]] |
||
Kiel registrite je 14:07, 1 mar. 2017
La leĝo de Boyle-Mariotte (aŭ leĝo de Boyle) diras, ke
Ekzemple, se la premo de unu gaso duobliĝas, la volumeno de la gaso reduktiĝos duone, kaj same inverse. La leĝon ektrovis en 1662 la irlanda fizikisto kaj ĥemiisto Robert Boyle.
Vidu ankaŭ
Eksteraj ligiloj
- http://www.thescubaguide.com/certification/boyles-law.aspx
- http://dbhs.wvusd.k12.ca.us/webdocs/GasLaw/Gas-Boyle-Data.html