Benzoilacetata acido
| Benzoilacetata acido | |||
 | |||
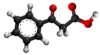
| Bastona kemia strukturo de la Benzoilacetata acido | |||
 | |||
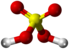
| Tridimensia kemia strukturo de la Benzoilacetata acido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 614-20-0 | ||
| ChemSpider kodo | 87610 | ||
| PubChem-kodo | 97045 | ||
| Fizikaj proprecoj | |||
| Aspekto | blanka solidaĵo | ||
| Molmaso | 164,16 g·mol−1 | ||
| Denseco | 1,242g cm−3[1] | ||
| Fandpunkto | 98 °C[2] | ||
| Bolpunkto | 349,1 °C | ||
| Refrakta indico | 1,556 | ||
| Ekflama temperaturo | 179,1 °C | ||
| Solvebleco | Akvo:Nesolvebla | ||
| Sekurecaj Indikoj | |||
| Riskoj | R22 R36/37/38 | ||
| Sekureco | S26 S36 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H315, H318, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P310, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Benzoilacetata acido aŭ C9H8O3 estas kemia kombinaĵo, apartenanta al la funkcia grupo el la aromataj acidoj de la benzoata acido kaj acetata acido. Benzoilacetata acido estas blanka solidaĵo, uzata kiel analiza reakciaĵo en kemiaj sintezoj kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Benzoilacetata acido estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Benzoilacetata acido reakcias kun fortaj oksidigagentoj kaj fortaj bazoj kaj posedas antifungajn kaj antibakteriajn proprecojn.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado per traktado de benzaldehido kaj kloroacetata acido:
Sintezo 2[redakti | redakti fonton]
- Preparado per interagado de la metila fenila ketono kaj kloroacetata acido:
Sintezo 3[redakti | redakti fonton]
- Preparado per reakcio inter la benzamido kaj kloroacetata acido:
Sintezo 4[redakti | redakti fonton]
- Preparado per reakcio inter la fenacila klorido kaj kloroformiata acido:
Sintezo 5[redakti | redakti fonton]
- Preparado per hidrolizo de la etila benzoilacetato:
Sintezo 6[redakti | redakti fonton]
- Preparado per reakcio inter etila benzoilacetato kaj sulfata acido:
Sintezo 7[redakti | redakti fonton]
- Preparado per hidratigo de amidoj:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Sapigo de la benzoilacetata acido:
Reakcio 2[redakti | redakti fonton]
- Reduktigo de la karboksilata acido:
Reakcio 3[redakti | redakti fonton]
- Klorigo de la karboksilata acido:
Reakcio 4[redakti | redakti fonton]
- Esterigo de la karboksilata acido:
Reakcio 5[redakti | redakti fonton]
- Reakcio kun tionila klorido:
Reakcio 6[redakti | redakti fonton]
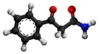
- Reakcio kun NH3:
Reakcio 7[redakti | redakti fonton]
- Intramolekula senhidratigo de la benzoilacetata acido
Literaturo[redakti | redakti fonton]
- Transition States of Biochemical Processes
- Advances in Catalysis
- The Alkaloids
- Biochemistry of Lipids, Lipoproteins and Membranes
- Journal of Chemical Society
- American Chemical Journal
- The Journal of Biological Chemistry
- RÖMPP Encyclopedia Natural Products





![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)





![{\displaystyle {\mathsf {{\xrightarrow[{-H_{2}O}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a1c5c3deca84c3438595dcf3dbb607cece3b72b3)




