Zirkonia (IV) hidroksido
| Zirkonia tetrahidroksido | ||
| Kemia formulo | ||
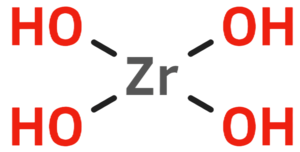 | ||
Zirkonia (IV) hidroksido | ||
 | ||
 | ||
| Zirkonito aŭ zirkonio: Erco de zirkonio. | ||
| Alternativa(j) nomo(j) | ||
| ||
| CAS-numero-kodo | 14475-63-9 12688-15-2 | |
| ChemSpider kodo | 19971949 | |
| PubChem-kodo | 84465 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka senforma solidaĵo | |
| Molmaso | 159,252g mol−1[1] | |
| Denseco | 3,25 g/cm−3 | |
| Fandpunkto | 550 °C (malkomponiĝas) | |
| Solvebleco | Akvo:0,2 g/L Solvebla en mineralaj acidoj | |
| Mortiga dozo (LD50) | >230 mg/kg (buŝe) | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P264+265, P271, P280, P302+352, P304+340, P305+351+338, P319, P321, P332+317, P337+317, P362+364, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Zirkonia (IV) hidroksido aŭ tetrahidroksido de zirkonio estas neorganika kombinaĵo apartenanta al la familio de la hidroksidoj, rezultanta el hidratagado de la zirkonia (IV) oksido aŭ hidrolizo de zirkoniaj (IV) saloj. Zirkonia (IV) hidroksido estas blanka senforma solidaĵo, malmulte solvebla en akvo uzata en la preparado de solidaj acidaj kataliziloj. Zirkonia (IV) hidroksido prezentas kvar hidroksilajn grupojn ligitajn al zirkoniatomo per jonaj ligaĵoj. Ĝi konsistas je 1 zirkoniatomo, 4 hidrogenatomoj kaj 4 oksigenatomoj.
Proprecoj
[redakti | redakti fonton]Zirkonia hidroksido estas unu el la plej uzataj zirkonio-komponaĵoj. Ĝi posedas grandan gravecon por la analiza kemio de zirkonio kaj teknologio. La aldono de amoniako aŭ alkalaĵoj al solvaĵoj de zirkoniaj saloj precipitigas (en la malvarmo) zirkonian hidroksidon kiel gelatinan blankan senforman restaĵon. Ĝi povas formiĝi ankaŭ per la hidrolizo de zirkoniaj saloj. Al zirkonia hidroksido oni ne povas atribui difinitan formulon. Ĝi estas hidratigita zirkonia duoksido, kies grado de hidratiĝo dependas de pluraj kondiĉoj. La hidroksido havas pli grandan gradon de hidratiĝo kaj disvastigo kiam precipitita malvarme en alkala medio, ol kiam formita per malrapida hidrolizo en malforte acida medio kiu estis varmigita.
Obee la nomenklaturon establitan por titanio kaj stano, la unua kunmetaĵo de zirkonio estis nomumita kiel ortozirkonia acido aŭ a-modifo, Zr(OH)4, kaj la dua kunmetaĵo kiel metazirkonia acido aŭ 3-modifo, ZrO(OH)2. La β-modifo akiriĝas post longedaŭra bolado aŭ starado dum longa tempo. Kiel metastanata acido, ĝi ne estas solvebla en acidoj.
Zirkonia hidrolizo komenciĝas je malalta pH kaj dependas forte de temperaturo, acideco, kaj la kvanto de zirkonio kaj de aliaj saloj. Zirkonia hidroksido komencas precipitiĝi en malvarme solvaĵo de klorida acida je pH = 1,9. Konsiderinda restaĵo akiriĝas ĉe pH = 3,4. En solvaĵoj de sulfata acido zirkonio precipitas je pH = 1,7 kaj finiĝas je pH = 4,2. En varmaj solvaĵoj la precipitaĵo de zirkonia hidroksido okazas ĉe pli alta pH (53). La hidroksido precipitita en tiuj kondiĉoj malrapide dissolviĝas sur varmigado en densaj mineralacidoj kaj dissolviĝas facile en diluita fluorida acido. Ĝi dissolviĝas rimarkinde en alkaloj, sed solvebleco malpliiĝas kun la reduktado de la alkala koncentriĝo.
Kiam precipitiĝas en la malvarmo, la hidroksido dissolviĝas facile en diluitaj mineralaj acidoj, en oksalata acido, same kiel en koncentritaj solvaĵoj de alkalaj metalaj karbonatoj kaj precipe en amonia karbonato. Krome, la hidroksido estas solvebla en forta alkalo en ĉeesto de hidrogena peroksido formanta perzirkonaton kiu precipitiĝas en ĉeesto de alkoholo.[1]
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Preparado de zirkonia (IV) hidroksido per traktado de zirkonia (IV) oksido kun akvo:
Reakcio 2
[redakti | redakti fonton]- Preparado de zirkonia (IV) hidroksido per traktado de zirkonia (IV) klorido kun natria hidroksido:
Reakcio 3
[redakti | redakti fonton]- Preparado de zirkonia (IV) hidroksido per hidrolizo de la plumban (IV) kloridon:
Reakcio 4
[redakti | redakti fonton]- Preparado de zirkonia (IV) oksido per senhidratigado de zirkonia (IV) hidroksido:
Reakcio 5
[redakti | redakti fonton]- Reakcio de zirkonia (IV) hidroksido kun klorida acido donante zirkonia (IV) klorido:
| Saloj de Zirkonio (IV) | |||
 |
 |
 |  |




![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)





![{\displaystyle {\mathsf {{\xrightarrow[{}]{200^{o}C}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/325e588959182bbc49a8fb0885c6b0757ce1dfc6)