Metila bikarbonato
| Metila bikarbonato | ||
 | ||
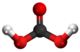
| Plata kemia strukturo de la Metila bikarbonato | ||
 | ||
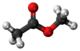
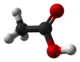
| Tridimensia kemia strukturo de la Metila bikarbonato | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 7456-87-3 | |
| ChemSpider kodo | 70939 | |
| PubChem-kodo | 78579 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora likvaĵo | |
| Molmaso | 76,052-1 | |
| Denseco | 1,216g/cm−3 | |
| Bolpunkto | 119,1 °C [1] | |
| Refrakta indico | 1,384[2] | |
| Ekflama temperaturo | 54,9 °C | |
| Solvebleco | Akvo:solvebla | |
| Mortiga dozo (LD50) | 5360 mg/kg (buŝe) | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Damaĝa substanco | |
| GHS Deklaroj pri damaĝoj | H225, H361 | |
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P280, P303+361+353, P370+378, P403+235, P501 | |
(25 °C kaj 100 kPa) | ||
Metila bikarbonato estas kemia kombinaĵo, apartenanta al la funkcia grupo de esteroj rezultanta el nekompleta esterigo de la karbonata acido kaj metanolo en ĉeesto de sulfata acido. Ĝi estas senkolora bruligebla likvaĵo uzata en kemiaj sintezoj kaj en la fabrikado de farmaciaĵoj. Kiel metiliga agento ĝi uzatas en la produktado de anilinoj, karboksilataj acidoj kaj fenoloj. La avantaĝo de la metila bikarbonato sur aliaj metiligagentoj tiaj kiaj jodometano kaj dumetila sulfato estas ĝia malalta tokseco. Bedaŭrinde, ĝi estas malforta metiligagento kiam komparata al aliaj tradiciaj reakciaĵoj. Ĝi ankaŭ uzatas kiel solvanto.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado per traktado de karbonata acido kaj metanolo:
Sintezo 2[redakti | redakti fonton]
- Preparado per traktado de karbona duoksido kaj metanolo:
Sintezo 3[redakti | redakti fonton]
- Preparado per traktado de karbonata acido kaj "metila bisulfido":
Sintezo 4[redakti | redakti fonton]
- Preparado per traktado de metila klorido kaj natria bikarbonato:
Sintezo 5[redakti | redakti fonton]
- Preparado per interagado de kalia bikarbonato kaj metila formiato:
Sintezo 6[redakti | redakti fonton]
- Preparado per acida interŝanĝo de karbonata acido kaj metila acetato:
Sintezo 7[redakti | redakti fonton]
- Preparado per duobla interŝanĝo de "izopropila bikarbonato" kaj metanolo:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Hidrolizo de la metila bikarbonato
Reakcio 2[redakti | redakti fonton]
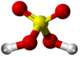
- Reakcio kun sulfata acido:
Reakcio 3[redakti | redakti fonton]
- Preparado de metila butanato per acida interŝanĝo inter metila bikarbonato kaj buterata acido:
Reakcio 4[redakti | redakti fonton]
- Preparado de metila benzoato per duobla interŝanĝo de metila bikarbonato kaj benzoata acido en acida medio:
Reakcio 5[redakti | redakti fonton]
- Malkomponado de la metila bikarbonato. La monoesteroj de la karbonata acido estas konsiderataj kiel malstabilaj kaj malkomponiĝas al alkoholo kaj karbona duoksido:[3]
Reakcio 6[redakti | redakti fonton]
- Reakcio kun sulfida acido
Reakcio 7[redakti | redakti fonton]
- Reakcio kun klorida acido:
Literaturo[redakti | redakti fonton]
- Bicarbonates—Advances in Research and Application
- The American Chemist
- Sports nutrition
- Trout and Salmon Culture: Hatchery Methods
- College Practical Chemistry
- Training course in water and sewage plant operations
- Raw Materials Development Laboratory Handbook of Analytical Methods




![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)




![{\displaystyle {\mathsf {{\xrightarrow[{}]{+[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/88fb0b03b975cfe42ff07b526c4bddf66812655c)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{[OH]^{-}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/258ce3c08df9dce17beda55311dbfb79464c8a40)
