Arsenata acido
Aspekto
| Arsenata acido | ||
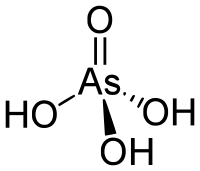 | ||
| Plata kemia strukturo de la Arsenata acido | ||
 | ||
| Tridimensia kemia strukturo de la Arsenata acido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 7778-39-4 | |
| ChemSpider kodo | 229 | |
| PubChem-kodo | 234 | |
| Merck Index | 15,785 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora aŭ blanka nebrulema likvaĵo | |
| Molmaso | 141942 g·mol−1 | |
| Denseco | 2.2g cm−3 | |
| Fandpunkto | −35.5 °C | |
| Bolpunkto | 120 °C (malkomponiĝas) | |
| Acideco (pKa) | 2.22 | |
| Solvebleco | Akvo:167 g/L | |
| Mortiga dozo (LD50) | 48 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R23/25 | |
| Sekureco | S45 S53 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo | ||
| GHS Signalvorto | ||
| GHS Deklaroj pri damaĝoj | H301, H312, H314, H318, H331, H350, H361, H400, H410 | |
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P301+310, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P308+313, P310, P311, P312, P321, P330, P363, P391, P403+233, P405, P501[1] | |
(25 °C kaj 100 kPa) | ||
Arsenata acido estas kemia kombinaĵo konsistanta je unu atomo de arseno, kvar atomoj je oksigeno kaj tri hidrogenatomoj. Ĝi estas senkolora substanco kaj analogaĵo de la fosfata acido, kies saloj kondutas sin tre simile. Arsenata acido ne povas esti izolita sed trovata nur en akva solvaĵo kie ĝi larĝe joniziĝas.
Kristalspecimenoj de arsenata acido senhidratiĝas kiam temperaturo altas pli ol 100 °C. Komercaj aplikadoj de arsenata acido estas limigitaj pro ĝia tokseco. Ĝi estas antaŭaĵo de vasta gamo da pesticidoj, pro tio ĝi estas uzata ankaŭ kiel ligno-konservaĵo, biocido kaj reakcianto en la sintezo de tinkturoj en organikaj arsenaj komponaĵoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Tiam kiam la akva solvaĵo estas abunde koncentrita, arsenata acido precipitiĝas tiel kiel etaj, senkoloraj, delikvaj kristaloj. Ĝi estas preparebla per interagado de la arsenata trioksido en akva solvaĵo en ĉeesto de nitrata acido:[2]
|
|
Sintezo 2
[redakti | redakti fonton]- Se la solvaĵo estas malpli diluita, N2O3 estiĝas anstataŭ NO.
|
|
Sintezo 3
[redakti | redakti fonton]|
|
Sintezo 4
[redakti | redakti fonton]- Arsenata acido povas sinteziĝi per reakcio inter duarsena trioksido, akvo kaj jodo:
|
|
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Arsenata acido malkomponiĝas ĉe altaj temperaturoj:
|
|
Reakcio 2
[redakti | redakti fonton]- Arsenata acido posedas oksidigajn proprecojn, kiu manifestiĝas nur en acida medio:
|
|
Literaturo
[redakti | redakti fonton]- Chemicalland21
- ChemNet
- Lewis' Dictionary of Toxicology
- Implementation of Arsenic Treatment Systems
- Wiley Guide to Chemical Incompatibilities







