Fosforamido
| Fosfora triamido | |||
| Kemia formulo | |||
 | |||
Fosforamido | |||
 | |||
| Alternativa(j) nomo(j) | |||
| |||
| CAS-numero-kodo | 13597-72-3 | ||
| ChemSpider kodo | 109920 | ||
| PubChem-kodo | 123317 | ||
| Fizikaj proprecoj | |||
| Aspekto | blanka solidaĵo | ||
| Molmaso | 95,041022 g mol−1 | ||
| Denseco | 1,491 g/cm−3[1] | ||
| Fandpunkto | 90,3°C [2] | ||
| Bolpunkto | 480°C | ||
| Refrakta indico | 1,5250 | ||
| Solvebleco | Akvo:solvebla | ||
| Mortiga dozo (LD50) | >500 mg/kg (buŝe) | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H410, H412 | ||
| GHS Deklaroj pri antaŭgardoj | P264, P264+265, P273, P280, P302+352, P305+351+338, P321, P332+317, P337+317, P362+364, P391, P501 | ||
(25 °C kaj 100 kPa) | |||
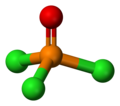
Fosforamido aŭ fosfora triamido estas organika kombinaĵo rezultanta el interagado de la fosforila klorido kaj amoniako. Ĝi estas blanka solidaĵo, solvebla en akvo. Fosforamido posedas 6 hidrogenatomojn, 3 nitrogenatomojn, 2 sulfuratomojn, kaj 1 fosforatomon. Fosforamido uzatas en kemiaj sintezoj kaj en la preparado de farmaciaĵoj.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado de la sulfida acido per traktado de fosforamido kaj sulfida acido:
Sintezo 2[redakti | redakti fonton]
- Preparado de la fosforamido per traktado de fosforila klorido kaj amoniako:
Sintezo 3[redakti | redakti fonton]
- Preparado de la fosforamido per traktado de fosfina oksido kaj kloramino:
Sintezo 4[redakti | redakti fonton]
- Preparado de la kloramino per traktado de fosfino kaj kloramino:





![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)






![{\displaystyle {\mathsf {{\xrightarrow[{}]{K_{2}Cr_{2}O_{7}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e7efdb10599cff1612b82cc073bcd5ba291d25eb)