Furanila klorido
| 2-Kloro-furano | |||
| Kemia formulo | |||
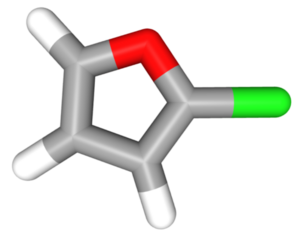 | |||
2-Kloro-furano | |||
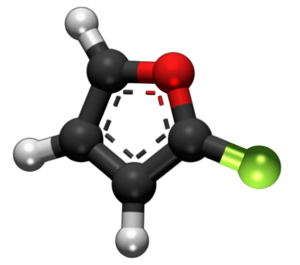 | |||
| Alternativa(j) nomo(j) | |||
| CAS-numero-kodo | 3187-94-8 | ||
| ChemSpider kodo | 121505 | ||
| PubChem-kodo | 137856 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora likvaĵo | ||
| Molmaso | 102,51992 g mol−1 | ||
| Denseco | 1,217 g/cm−3[1][2] | ||
| Fandpunkto | -22,1°C [3] | ||
| Bolpunkto | 74°C[1] | ||
| Refrakta indico | 1,4569[4][5] | ||
| Ekflama temperaturo | 7,32°C[3] | ||
| Solvebleco | Akvo:malkomponiĝas | ||
| Mortiga dozo (LD50) | 572 mg/kg (buŝe) | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H315, H319 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P264, P280, P370+378, P337+313, P305+351+338, P362+364, P303+361+353, P332+313, P403+235, P501 | ||
(25 °C kaj 100 kPa) | |||
Furanila klorido aŭ 2-kloro-furano estas organika kombinaĵo rezultanta el interagado de la kloro kaj furano. Ĝi estas senkolora likvaĵo, kiu malkomponiĝas en akva medio. Furanila klorido posedas 4 karbonatomojn, 3 hidrogenatomojn kaj 1 kloratomon.
2-Klorofurano estas kemia kunmetaĵo apartenanta al la familio de la ciklaj nesaturitaj alkoholoj. Ĝi estas heterocikla kunmetaĵo kiu enhavas furanan ringon kun kloratomo alkroĉata al ĝi. 2-Klorofurano estas kutime uzata en scienca esplorado kiel komenca materialo por la sintezo de diversaj organikaj kombinaĵoj.
2-Klorofurano havas ampleksan gamon de sciencaj esplor-aplikoj. Ĝi estas ofte uzata kiel komenca materialo por la sintezo de diversaj organikaj substancoj kiel farmaciaĵoj, agrokemiaĵoj kaj aromataĵoj. Ĝi ankaŭ estas uzata kiel solvanto en la sintezo de aliaj organikaj kombinaĵoj. Aldone, 2-Klorofurano estas uzata kiel reakciaĵo en organika sintezo por enkonduki kloran atomon en organikajn molekulojn.
La mekanismo de ago de 2-Klorofurano ne estas bone komprenita. Tamen, ĝi verŝajne funkcias kiel elektrofilo pro la ĉeesto de la kloratomo. Tio igas ĝin tre reakciema direkte al nukleofiloj, kio permesas al ĝi esti utiligata kiel reakciaĵo en organika sintezo.
Estas limigitaj informoj haveblaj pri la biokemiaj kaj fiziologiaj efikoj de 2-Klorofurano. Tamen, ĝi pruviĝis havi kelkajn toksajn efikojn al vivantaj organismoj. Studoj montris, ke eksponiĝo al 2-Klorofurano povas kaŭzi hepatan damaĝon kaj malpliigon de korpa pezo en ratoj. Plia esplorado estas necesa por plene kompreni la biokemiajn kaj fiziologiajn efikojn de 2-Klorofurano.
Unu el la ĉefaj avantaĝoj de uzado de 2-Klorofurano en laboratoriaj eksperimentoj estas ĝia alta reakciemo al nukleofiloj. Tio igas ĝin utila reakciilo en organika sintezo. Aldone, la sintezo de 2-Klorofurano estas relative simpla kaj donas produkton kun alta pureco. Tamen, ekzistas ankaŭ iuj limigoj al uzado de 2-Klorofurano en laboratorio-eksperimentoj. Ĝi estas venena kunmetaĵo kaj devas esti pritraktata zorge. Aldone, ĝi ne estas tre solvebla en akvo, kio povas malfaciligi ĝin uzi en akvaj reakcioj.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado de la kloro per traktado de furano kaj kloro:
Sintezo 2[redakti | redakti fonton]
- Preparado de la klorida acido per traktado de furano kaj klorida acido:
Sintezo 3[redakti | redakti fonton]
- Preparado de la kloro per traktado de 2-metilfurano kaj kloro:
Sintezo 4[redakti | redakti fonton]
- Preparado de la furanila klorido per traktado de furano kaj fosfora triklorido:
Sintezo 5[redakti | redakti fonton]
- Preparado de la fosfora kvinklorido per traktado de furano kaj fosfora kvinklorido:





![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)