Trikloramino
| Trikloramino | |||||
 | |||||
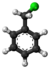
| Plata kemia strukturo de la Trikloramino | |||||
 | |||||
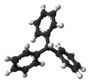
| Tridimensia kemia strukturo de la Trikloramino | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 10025-85-1 | ||||
| ChemSpider kodo | 55361 | ||||
| PubChem-kodo | 61437 | ||||
| Merck Index | 15,6689 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | toksa, potence eksplodema, flava oleeca likvaĵo kun penetranta malagrabla odoro | ||||
| Molmaso | 120,357 g·mol-1 | ||||
| Denseco | 1,653g cm−3 | ||||
| Fandpunkto | -40°C | ||||
| Bolpunkto | 71°C | ||||
| Memsparka temperaturo | 93 °C | ||||
| Solvebleco | Akvo:r, soluble in benzene, chloroform, CCl4, CS2, PCl3 g/L | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R19 R27/28 R45 | ||||
| Sekureco | S7 S22 S26 S36 S37 S39 S45 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H290, H314, H315, H319, H335, H372, H412 | ||||
| GHS Deklaroj pri antaŭgardoj | P234, P260, P261, P264, P270, P271, P273, P280, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P310, P314, P321, P332+313, P337+313, P362, P363, P403+233, P404, P405, P501 | ||||
(25 °C kaj 100 kPa) | |||||
Trikloramino aŭ NCl3 estas neorganika klora kombinaĵo de nitrogeno, toksa, potence eksplodema, flava oleeca likvaĵo kun penetranta malagrabla odoro uzata en eksplodaj reakcioj en kemiaj sintezoj, kiel amoniaka klorderivaĵo. Kiel oni povas konstati trikloramino devenas el amoniako kie ĉiuj hidrogenatomoj estis anstataŭataj de kloratomoj. Trikloramino estas solvebla en benzeno, karbona kvarklorido, karbona dusulfido kaj fosfora triklorido.
Nitrogena triklorido estas irita al mukoza membranoj kaj larmigagento. La pura substanco estas potence eksplodema kaj sensiva al sunlumo, varmo kaj, al milda ŝoko kaj organikaj komponaĵoj. Pierre Louis Dulong ĝin preparis en 1812, kaj tiu malkovro kostis al li du fingrojn. En 1813, la sama eksplodo okazis kun Humphry Davy kiu dum kelka tempo blindiĝis. Pro tio li devis dungi Michael Faraday kiel sia asistanto, kiu cetere suferis la saman eksplodon. Pli malfrue, Antoine-Jérôme Balard, Rudolf Christian Böttger kaj Hermann Kolbe trovis aliajn metodojn.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de amonia nitrato kaj kloro:
Sintezo 3
[redakti | redakti fonton]- Sintezo per traktado de amonia karbonato kun kloro::
Sintezo 4
[redakti | redakti fonton]- Preparado per agado de amonia klorido kaj klora duoksido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Makomponado de trikloramino:
Reakcio 2
[redakti | redakti fonton]- Hidrolizo de de trikloramino:
Reakcio 3
[redakti | redakti fonton]- Reakcio de kloramino kaj kalia hidroksido:
Reakcio 4
[redakti | redakti fonton]- Klorigo de terciaraj karbonoj:
Reakcio 5
[redakti | redakti fonton]- Transformado de alkoholoj en kloridojn:
Kemiistoj kiuj esploris trikloraminon
[redakti | redakti fonton]-
Hermann Kolbe (1818-1884) -
Pierre Louis Dulong
(1785-1838) -
Humphry Davy (1778-1829) -
Antoine-Jérôme Balard
(1802-1876) -
Rudolf Christian Böttger
(1806-1881) -
Michael Faraday (1791-1867)
Vidu ankaŭ
[redakti | redakti fonton]Literaturo
[redakti | redakti fonton]- Distribution Generated Taste-and-odor Phenomena
- Some Drinking-water Disinfectants and Contaminants, Including Arsenic
- Advances in Taste-and-odor Treatment and Control
- Food Taints and Off-Flavours
- Seasonal Chlorination Practices and Impacts to Chloraminating Utilities
- Issues in Environment, Health, and Pollution









![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)