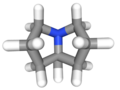
Pirolizidino
| Heksahidropirolizino | ||||
| Kemia formulo | ||||
 | ||||
Heksahidropirolizino | ||||
 | ||||
| Alternativa(j) nomo(j) | ||||
| CAS-numero-kodo | 643-20-9 | |||
| ChemSpider kodo | 12039 | |||
| PubChem-kodo | 12558 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora likvaĵo | |||
| Molmaso | 111,18696 g mol−1 | |||
| Denseco | 0,975 g/cm−3[1] | |||
| Fandpunkto | -9,9°C [2] | |||
| Bolpunkto | 145,8°C [3] | |||
| Refrakta indico | 1,4731[4] | |||
| Ekflama temperaturo | 34,2°C [5] | |||
| Solvebleco | Akvo:3,8 g/L | |||
| Mortiga dozo (LD50) | 381 mg/kg (buŝe) | |||
| GHS etikedigo de kemiaĵoj | ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H225, H302, H314 | |||
| GHS Deklaroj pri antaŭgardoj | P501, P270, P240, P210, P233, P243, P241, P242, P264, P280, P370+378, P303+361+353, P301+330+331, P363, P301+312, P304+340, P305+351+338, P310, P330, P403+235, P405 | |||
(25 °C kaj 100 kPa) | ||||
Pirolizidino aŭ heksahidropirolizino estas organika kombinaĵo aŭ alkaloido trovata en plantoj el diversaj specioj. Ĝi estas senkolora likvaĵo, malmulte sovebla en akvo. Pirolizidino posedas 7 karbonatomojn, 13 hidrogenatomojn kaj 1 nitrogenatomon. Pirolizidino uzatas en kemiaj sintezoj kaj en la preparado de pesticidoj, farmaciaĵoj kaj industriaĵoj. Pyrolizidino estas alkaloido trovata en naturo, ĝenerale en multaj el la plantoj de la familioj Boragacoj, Compositae kaj Leguminosae. La alkaloido pirolizidino estas hepatotoksa, tio estas, ĝi povas damaĝi la hepaton.
Proprecoj
[redakti | redakti fonton]Pirolizidinaj alkaloidoj (PA) estas naturaj toksinoj kiujn plantoj sintezas en sia sekundara metabolo kiel defenda mekanismo kontraŭ plantomanĝantoj. Ĉirkaŭ 600 malsamaj PA-oj estas priskribitaj en multaj plantoj, la granda plimulto de kiuj apartenas al 5 botanikaj familioj, kiuj produktas malsamajn specojn de alkaloidoj: Boragacoj, Compositae kaj Leguminosae, Orkidacoj kaj Apocynaceae.
El tiuj familioj oni produktas malsamajn AP-ojn, inter kiuj elstaras tiuj de la tipo senecionino, likopsamino, heliotrino kaj monokrotalino pro sia ĉeesto en manĝaĵoj kaj nutraĵoj el plantdeveno.
La baza strukturo estas la pirolizidina ringo, konsistanta el du pirolaj ringoj kunfanditaj kun nitrogenatomo kiel ponto. Ili estas kutime esteroj formitaj de strukturo konata kiel ""necina bazo"" kaj acida parto nomata ""necina acido"".
Ekzistas 4 necinaj bazoj: retronecino, heliotridino, otonecino kaj platinecino.
Ili havas duoblan ligon en pozicioj 1 kaj 2 de la ringo, esterigado de la hidroksimetilo en la pozicio 1 kaj unu hidroksilo en pozicio 7 kaj alkilaj ĉenoj kiuj esterigas la menciitajn grupojn. Tiuj alkilaj ĉenoj havas branĉojn, kiuj faciligas al la pirolizidinringo malkomponiĝi laŭ tre reakciemajn pirolajn ringojn kun alta reakciemo, kaŭzante toksecon.
Biologia aktiveco
[redakti | redakti fonton]La nivelo de tokseco dependas fundamente de ĝia kemia strukturo, la individuigitaj vojoj en alkaloida metabolo, la niveloj pri sentokseco kaj la variaĵoj de ĉiu individuo. Por ke ili estu venenaj, ili devas havi duoblan ligon inter pozicioj 1 kaj 2 kaj estergrupo en la pozicio C-7, en la pozicio C-9 aŭ en ambaŭ pozicioj de la necina bazo.
Pirolizidinaj alkaloidoj estas konsiderataj antaŭtoksinoj, do por produkti toksecon ili devas esti aktivigitaj per hepata metabolo per la mekanismo de oksidiva sentokseco.
Tiamaniere ke, la alkaloidoj, ingestitaj en sia terciara formo, estas transformitaj en pirolaj metabolitoj danke al la citokromo P450 monooksigenaza enzimo. Krome, kiam ili estas konsumitaj en sia netoksa formo, tio estas, en formo de nitrogenaj oksidoj kaj ne libera bazo aŭ terciara alkaloido (toksa formo), ili ankaŭ povas esti reduktitaj al sia terciara alkaloido (toksa formo), sorbataj kaj poste aktivigataj per la hepataj vojoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado de la formiila klorido per traktado de 5-okso-pirolidinilpropionata acido kaj fosgeno sekvata per reduktado de la ketono formita:






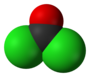
![{\displaystyle {\mathsf {{\xrightarrow[{2\,H_{2}O}]{4\,[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/184270af9d5cb06ee7c32d40739d99b579eda892)