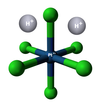
Stana (IV) klorido
| Tetraklora stanato | |||||
| Kemia formulo | |||||
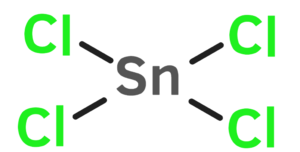 | |||||
Tetraklora stanato | |||||
 | |||||
| Alternativa(j) nomo(j) | |||||
| Stanika muriato | |||||
| CAS-numero-kodo | 7646-78-8 | ||||
| ChemSpider kodo | 22707 | ||||
| PubChem-kodo | 24287 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora aŭ blanka solidaĵo | ||||
| Molmaso | 260,49g mol−1 | ||||
| Denseco | 2,226 g/cm−3[1] | ||||
| Fandpunkto | -33°C [2][3] | ||||
| Bolpunkto | 114,1°C [4] | ||||
| Refrakta indico | 1,5120[5] | ||||
| Ekflama temperaturo | 1,1°C [6] | ||||
| Solvebleco | Akvo:reakcias Solvebla en alkoholo, benzeno, tolueno, kloroformo, acetono, karbona tetraklorido, benzino and karbona dusulfido. | ||||
| Mortiga dozo (LD50) | >2000 mg/kg (buŝe) | ||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H290, H302+332, H302, H312, H314, H317, H318, H319, H332, H335, H373, H400, H410 | ||||
| GHS Deklaroj pri antaŭgardoj | P234, P260, P261, P264, P264+265, P270, P271, P272, P273, P280, P301+317, P301+330+331, P302+352, P302+361+354, P304+340, P305+351+338, P305+354+338, P316, P317, P319, P321, P330, P333+313, P337+317, P362+364, P363, P390, P391, P403+233, P405 | ||||
(25 °C kaj 100 kPa) | |||||
Stana (IV) klorido aŭ muriato de stano (IV) estas neorganika kombinaĵo apartenanta al la familio de la kloridoj, rezultanta el interagado de la stana (IV) hidroksido kaj klorida acido. Stana (IV) klorido estas reakciema en akvo, solvebla en etanolo, acetono, etero, tetrahidrofurano kaj nesolvebla en ksilolo. Stana (IV) klorido prezentas kvar klorajn jonojn ligitajn al stanatomo. Ĝi konsistas je 1 stanatomo, 4 kloratomoj, kaj uzatas en kemiaj sintezoj. Stana tetraklorido estis unue malkovrita de Andreas Libavius (1550-1616) kaj estis konata kiel spiritus fumans libavii (fumeganta spirito de Libavius).
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Preparado de stana (IV) klorido per traktado de stana (II) klorido kun kloro:
Reakcio 2[redakti | redakti fonton]
- Preparado de stana (IV) klorido per traktado de klorida acido kun stano:
Reakcio 3[redakti | redakti fonton]
- Preparado de stana (II) klorido per malkomponado de stana (IV) klorido:
Reakcio 4[redakti | redakti fonton]
- Preparado de stana (IV) klorido per traktado de klorida acido kun stano:
Reakcio 5[redakti | redakti fonton]
- Preparado de stana (IV) klorido per malkomponado de la heksaklorostanata acido:
Reakcio 6[redakti | redakti fonton]
- Preparado de kalia tetraklorostanato (II)[7] per traktado de stana (IV) klorido kun kalia klorido
Reakcio 7[redakti | redakti fonton]
- Preparado de heksaklorostanata acido per interagado de stana (IV) klorido kaj klorida acido:[8]







![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)




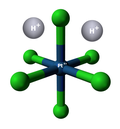
![{\displaystyle {\mathsf {{\xrightarrow[{}]{varmo}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/39f1c6c7ab29f583de5842596076f1dac2b5b61a)