Metastabileco
Metastabileco estas ĝenerala scienca koncepto kiu priskribas statojn de delikata ekvilibro. Sistemo estas en metastabila stato kiam ĝi estas en ekvilibro (ne ŝanĝanta kun tempo) sed estas ebleco por ĝi fali en sube energiajn statojn pro nur malgranda interago. Ĝi estas analoga al estado je la fundo de malgranda valo kiam estas pli profunda valo proksime - loka stabileco de sistemo je loka (sed ne malloka) minimumo de potencialo.
Preskaŭ ĉiu sistemo povas demonstracii metastabilecon, sed ĝi estas plej komuna en sistemoj de malforte interagantaj partikloj en fiziko kaj kemio.
En volumenaĵa materio
[redakti | redakti fonton]
Sabloamasoj estas sistemo kiu povas havi metastabilecon se estas kruta inklino aŭ tunelo. Sablaj grajnoj formas amason pro frotado. Estas por tuta granda sabla amaso esti stabila, sed la aldono de sola grajno kaŭzas ke grandaj partoj de ĝi kolapsas.
Lavango estas konata problemo kun grandaj amasoj de neĝaj kaj glaciaj kristalaj sur krutaj inklinoj. En sekaj kondiĉoj, neĝa inklino agas simila al sabloamasoj. Tuta monta flanko kovrita de neĝo povas subite ekgliti pro skiisto, bruego aŭ vibrado.
En fazoj de materio
[redakti | redakti fonton]Metastabilaj fazoj de materio inkluzivi tiuj kiu estas supermalvarmigita aŭ supervarmigita. Ekzemple, supermalvarmigita akvo povas ekzisti en likva formo je temperaturoj pli sube de frosta temperaturo, kaj resti tia ĝis ekstera interago (vibrado aŭ enkonduko de sema partiklo) kaŭzanta la akvon kristaliĝi.
En elektronikaj cirkvitoj
[redakti | redakti fonton]
Metastabileco en elektroniko estas kutime vidata kiel problemo. Ŝanĝiĝo de tensioj kaj kurentoj en cirkvito estas supozita al finaranĝi en unu el certa malgranda kvanto de dezirataj statoj, sed se la cirkvita emas al metastabileco, ĝi povas resti tro longe aŭ por ĉiam en nedezirata stato.
Se ambaŭ enenigoj R kaj S de RS-baskulo egalas al 1, ĝi devus esti en unu el du nesimetriaj stabilaj statoj. Unu stabila stato estas Q=0, Q=1, la alia estas Q=1, Q=0. Sed se la cirkvito estas sifuĉe simetria, do post ŝanĝo de enenigoj de R=0, S=0 al R=1, S=1, ĝi estos relative longe en simetria stato kiam Q=Q, kaj la valoro de Q kaj Q estas meza inter logikaj 0 kaj 1.
En kemiaj sistemoj
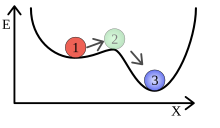
[redakti | redakti fonton]En kemio, sistemo de atomoj aŭ molekuloj engaĝanta ŝanĝon en fazo de materio, kristalsistemo aŭ kemia ligo povas esti en metastabila stato, kiu povas daŭri por relative longan tempon. Molekulaj vibradoj pro varmo faras ke kemiaj sistemoj je la energio ekvivalenta al la supro de ronda monteto estas mallongdaŭra. Metastabilaj statoj kiu ekzistas por multaj sekundoj aŭ eĉ jaroj estas trovitaj en energiaj valoj kiuj tamen estas ne la plej subaj eblaj valoj (punkto 1 en ilustraĵo).
Tre kutima ekzemplo estas lignaĵo sur aero. La stabila stato de ĝi (3) estas reakciigita kun oksigeno de aero, en formo de akvo H2O kaj karbona duoksido CO2. Tamen por ke ĝi trafu ĉi tiun staton, necesas trairi monteton (2), kio estas ke necesas bruligi la lignaĵon, varmiginte sufiĉe almenaŭ ĝian parton.
Kiel la alia ekzemplo, diamanto estas metastabila formo de karbono je norma temperaturo kaj premo. Ĝi povas esti konvertita al grafito kun eligo aldona energio, sed nur post superigo de dinamika ekzemplera energio - la monteto (2).
En nuklea fiziko
[redakti | redakti fonton]Atomkerno povas esti en malsamaj energiaj statoj. Iuj el ĉi tiuj ŝtatoj estas metastabila, sciataj kiel nukleaj izomeroj, kun signifo ke tie povas esti relative longe vivantaj kernoj de la sama izotopo en malsamaj energiaj ŝtatoj.
En kvantummekaniko
[redakti | redakti fonton]Sistemoj kiu estas priskribita per kvantummekaniko povas havi metastabilajn statojn. En ĉi tiu okazo, la metastabila stato povas disfali al malloka minimuma stato per kvantumomekanikaj efikoj, ekzemple tunela efiko. Ekzemploj estas radioaktivaj izotopoj kaj la pli supre menciitaj nukleaj izomeroj.
