Ciklopropila cianido
| Ciklopropila cianido | |||
 | |||
| Plata kemia strukturo de la Ciklopropila cianido | |||
 | |||
| Tridimensia kemia strukturo de la Ciklopropila cianido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 5500-21-0 | ||
| ChemSpider kodo | 71940 | ||
| PubChem-kodo | 79637 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora ĝis palflava likvaĵo | ||
| Molmaso | 67.0892 g·mol−1 | ||
| Denseco | 0.911 g cm−3 | ||
| Fandpunkto | −25 °C | ||
| Bolpunkto | 135 °C | ||
| Refrakta indico | 1,4210 | ||
| Ekflama temperaturo | 40 °C | ||
| Memsparka temperaturo | 182.7 °C | ||
| Solvebleco | Akvo:Miksebla | ||
| Mortiga dozo (LD50) | 1.2 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Risko | R10 R23/24/25 R36/37/38 | ||
| Sekureco | S16 S23 S26 S36/37/39 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[1] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H226, H301+311+331 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P280, P302+352, P312, P304+340, P370+378 | ||
(25 °C kaj 100 kPa) | |||
Ciklopropila cianido estas la plej eta karbonringa molekulo kun cianida grupo (-C≡N) ligita al la ringo. Ĝi estas ĉefe konata pro ĝia uzo en disvolvado de eksperimentoj kun mikroonda spektroskopio, rotacia spektroskopio kaj fotodissociiĝo.
En 1958, ciklopropila cianido estis unue esplorita pro ĝia rotacia spektro far la kemiistoj James P. Friend kaj B. P. Dailey. Aldona eksperimento kun la ciklopropila cianido estas la priskribado de la dupolara momento de la molekuloj per spektroskopiaj metodoj fare de Carvalho, en 1967.
| Izomerio - C4H5N | ||||
 |
 |

| ||
Sintezo
[redakti | redakti fonton]- Ciklopropila cianido povas esti facile preparata per interagado de la sodamido kun δ-klorobutironitrilo en likva amoniako-etera solvaĵo:[2]

Reakcio
[redakti | redakti fonton]Kiam varmigita al 660-760K kaj subpreme de 2-89torr, ciklopropila cianido iĝas cis kaj trans krotonitrilo kaj alilaj cianidoj, kun iom da metakrilonitrilo. Ĉi-izomeriga reakcio okazas pro la duradikala mekanismo, rezultante en la formado de liberaj radikaloj kaj malfermado de la trikarbona ringo. La radikaloj tiam reakcias por estigi karbono-karbonan duoblajn ligilojn.

Literaturo
[redakti | redakti fonton]- ACS Publications
- the NIST WebBook
- Chemical Book
- Alicyclic Chemistry, W. Parker
- Handbook of Phase Transfer Catalysis, Y. Sasson, Ronny Neumann
Kunrilataj kemiaĵoj
[redakti | redakti fonton]-
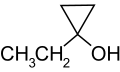
Etila ciklopropanolo -
Metil-etil-ciklopropano -
Ciklopropanoduolo -
Metil-ciklopropano -
Dumetilciklopropanolo -
Dumetil-ciklopropanono
Vidu ankaŭ
[redakti | redakti fonton]- Propano
- Ciklopropano
- Ciklopropano-karboksilata acido
- Propanoata acido
- Propionaldehido
- Propanolo
- Propanoata acido
Referencoj
[redakti | redakti fonton]- ↑ Sigma Aldrich
- ↑ A Survey of American Chemistry, National Research Council (U.S.). Division of Chemistry and Chemical Technology