Etileno-glikolo
| Etileno-glikolo | |||
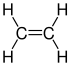
| Plata kemia strukturo de la Etileno-glikolo | |||
 | |||
| Tridimensia kemia strukturo de la Etileno-glikolo | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 107-21-1 | ||
| ChemSpider kodo | 13835235 | ||
| PubChem-kodo | 174 | ||
| Merck Index | 15,3852 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora senodora likvaĵo | ||
| Molmaso | 62,068 g·mol−1 | ||
| Denseco | 1,1132g cm−3 | ||
| Fandpunkto | -12.9 °C | ||
| Bolpunkto | 197.3 °C | ||
| Refrakta indico | 1,4318 | ||
| Ekflama temperaturo | 115 °C | ||
| Memsparka temperaturo | 398 °C | ||
| Acideco (pKa) | 14,22 | ||
| Solvebleco | Akvo:Tute solvebla | ||
| Mortiga dozo (LD50) | 4700 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R22 R36 | ||
| Sekureco | S26 S36 S37 S39 S45 S53 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝo | ||
| GHS Deklaroj pri damaĝoj | H315, H320, H332, H335, H336, H370[1] | ||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P270, P271, P280, P302+352, P304+312, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Etileno-glikolo estas organika kombinaĵo klasita kiel saturita du-alkoholo, senkolora kaj senodora likvaĵo kun dolĉa gusto, uzata en anti-glaciigaj formulaĵoj. Ĝi estas modere toksa. Etileno-glikolo helpas konservi la veturil-motoron kontraŭ glaciigo en vintro kaj agas kiel glaciigagento por reduktado de trovarmo en somero. Etileno-glikolo ankaŭ estas krudmaterialo en la produktado de vasta gamo da produktoj inkluzive de poliesteraj fibroj por vestaĵoj, remburaĵoj, tapiŝoj kaj kapkusenoj.
Sintezo[redakti | redakti fonton]
- Etileno-oksido estas preparata per kataliza hidratigo la etileno, kiu siavice estas hidratigita al etileno-glikolo:
  |
Ĉi-reakcio povas kataliziĝi de acidoj kaj bazoj, aŭ ankaŭ povas okazi en neŭtrala medio sub altaj temperaturoj. La plej alta rendimento de etileno-glikolo povas okazi en acida aŭ neŭtrala medioj kun larĝa troo da akvo. Ĉiujare pli ol 7 milionoj da tunoj de etileno-glikolo produktatas.
Literaturo[redakti | redakti fonton]
- Chemical Book
- Centroj por Kontrolo kaj Preventado de Malsanoj
- The Chemical Company
- Merck Millipore
- Ethylene Glycol Production from Carbon Dioxide - Cost Analysis - MEG E21A, Intratec Solutions
- Encyclopaedia of Occupational Health and Safety: Guides, indexes, directory, Jeanne Mager Stellman
- Clinical Environmental Health and Toxic Exposures, John Burke Sullivan, Gary R. Krieger





