Amonia sulfato
| Amonia sulfato | |||
 | |||
| Bastona kemia strukturo de la Amonia sulfato | |||
 | |||
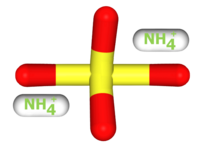
| Tridimensia strukturo de la Amonia sulfato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 7783-20-2 | ||
| ChemSpider kodo | 22944 | ||
| PubChem-kodo | 24538 | ||
| Merck Index | 14,555 | ||
| Fizikaj proprecoj | |||
| Aspekto | maldikaj blankaj granuloj aŭ kristaloj | ||
| Molmaso | 132.14 g·mol−1 | ||
| Denseco | 1.77 g cm−3 | ||
| Fandpunkto | inter 235 °C k 280 °C | ||
| Bolpunkto | ne disponebla | ||
| Refrakta indico | 1,3960 | ||
| Ekflama temperaturo | ne brulema | ||
| Memsparka temperaturo | ne brulema | ||
| Acideco (pKa) | 16.6 | ||
| Solvebleco | Akvo: | ||
| Mortiga dozo (LD50) | 2840 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Risko | R10 R22 R37/37/38 | ||
| Sekureco | S26 S36 S37/39 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[1] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H312, H315, H319, H402 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P262, P273, P302+352, P305+351+338, P501 | ||
(25 °C kaj 100 kPa) | |||
Amonia Sulfato estas salo de Amonio de la sulfata acido. Ĝi estas industrie produktita per rekta reakcio inter sulfata acido kaj amoniako kun emisio de varmo.
Je media ordinara temperaturo ĝi prezentiĝas kiel blankeca-senkolora kaj senodora solido. Ĝi estas utiligita en la kemia industrio kaj ankaŭ kiel sterko. Fakte, inter la ĝiaj utiligoj elstaras tiu de la sterkumado de alkalaj terenoj. En la tereno la amonia jono estas allasita kaj formas etan kvanton de acido malpliigante la pH de la tereno kun pliigo de kvanto de azoto.[2]
Ĝi povas esti produktita, ekzemple, per transŝanĝigo de gaso solvita en likvido al fazo gasa (angle: stripping) de la amoniako entenata en la rubeja “perkolato” (likvido filtriĝinta tra la rubeja maso), neŭtraligita per sulfata acido, post ĝiaj kontencentrado kaj kristalizado.
Amonia sulfato ekzistas en naturo en la rara mineralo nomata Maskagnito en la vulkanaj fumaroloj.
Vidu ankaŭ[redakti | redakti fonton]
Notoj[redakti | redakti fonton]
- ↑ Safety Data Sheet
- ↑ La uzo, tamen, de amonia sulfato prezentas malavantaĝojn pro ĝia eta enhavo de azoto kompare kun la amonia nitrato, kies utiligo, tamen, pezus pro la kostoj.
| ||||||





