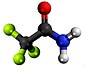
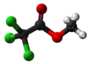
Metila trifluoroacetato
Etoso
| Metila trifluoroacetato | ||||
 | ||||
| Plata kemia strukturo de la Metila trifluoroacetato | ||||
 | ||||
| Tridimensia kemia strukturo de la Metila trifluoroacetato | ||||
Alternativa(j) nomo(j)
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 431-47-0 | |||
| ChemSpider kodo | 9509 | |||
| PubChem-kodo | 9893 | |||
| Merck Index | 15,9847 | |||
| Fizikaj proprecoj | ||||
| Aspekto | travidebla likvaĵo bruligebla, koroda kaj rapidbola | |||
| Molmaso | 128,0498-1 | |||
| Denseco | 1,5351g/cm−3 | |||
| Fandpunkto | -15,4 °C | |||
| Bolpunkto | 72,4 °C | |||
| Refrakta indico | 1,298 | |||
| Ekflama temperaturo | -7,2 °C | |||
| Solvebleco | Akvo:8 g/L | |||
| Mortiga dozo (LD50) | 1200 mg/kg (buŝe) | |||
| GHS etikedigo de kemiaĵoj | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H225, H314, H318 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P242, P243, P264 | |||
(25 °C kaj 100 kPa) | ||||
Metila trifluoroacetato aŭ C3H3F3O2 estas organika flurora kombinaĵo de acetata acido kun metanolo, senkolora, brulema, koroda likvaĵo uzata en kemiaj sintezoj kiel laboratoria reakciaĵo por fluorigoj kaj acetiligoj. Metila derivaĵo de la trifluoroacetata acido, ĝi estas uzata kiel insekticido kaj fungicido, toksa substanco kun iritaj proprecoj al haŭto, okuloj kaj per inhalado kaj per ingestado. Metila trifluoroacetato estas solvebla en akvo, alkoholo, etero, benzeno, kloroformo, heksano kaj acetono. Ĝi dissolvas proteinojn kiam miksita kun likva sulfura duoksido.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per interagado de trifluoroacetata acido kaj metanolo:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de acetata acido, trifluoramino kaj metanolo:
Sintezo 3
[redakti | redakti fonton]- Preparado per reakcio inter metila trijodoacetato kaj fluoro:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la metila trifluoroacetato:
Reakcio 2
[redakti | redakti fonton]- Reakcio de metila trifluoroacetato kun cianogeno:
Reakcio 3
[redakti | redakti fonton]- Preparado de trifluoroacetamido:
Reakcio 4
[redakti | redakti fonton]- Preparado de metila trikloroacetato:
Vidu ankaŭ
[redakti | redakti fonton]- Trifluoroacetatoj
- Trikloroacetata acido
- Metila trikloroacetato
- Metila trijodoacetato
- Metila tribromoacetato
Referencoj
[redakti | redakti fonton]- ↑ Synquest Laboratories[rompita ligilo]







![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)