Fluoro
Etoso
Fluoro estas kemia elemento de la perioda tabelo kun la simbolo F kaj atomnumero 9.
- Atompezo: 18,9984
- Kemia Serio: halogeno
- Specifa Pezo: 1,108 (likva)
- Fandopunkto: -219,67 oC
- Bolpunkto: -188,12 oC
- Eltrovinto: Moissan
Kemiaj kombinaĵoj de fluoro
[redakti | redakti fonton]Kun bildoj
[redakti | redakti fonton]-
Fluoreno -
Fluorenono -
Fluoroborata acido -
CHF3 -
Fluorosulfata acido -
Heksafluoro
benzeno -
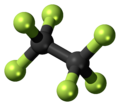
Heksafluoro
etano -
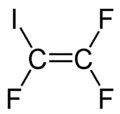
Jodo-trifluoro-etileno -
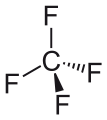
Karbona kvarfluorido -
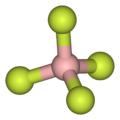
H3OBF4 -
Kvarfluorometano -
p-fluorobenzoata acido -
H2SiF6 -
Tionila fluorido -
Trifluorometila hipofluorito
Sen bildoj
[redakti | redakti fonton]- Amonia heksafluoro-antimonato
- Amonia heksafluoro-arsenato
- Amonia heksafluoro-platenato
- Amonia kvarfluoro-aluminiato
- Amonia kvarfluoro-antimonato
- Fluoro-metano-sulfonata acido
- Fluoroetano
- Fluorosulfata acido
- Fosfora kvinfluorido
- Fosfora trifluorido
- Kalia fluoro-silikato
- Natria dufluorofosfato
- Natria heksafluoro-antimonato
- Natria heksafluoro-arsenato
- Natria unufluorofosfato
- Nitrila fluorido
- Nitrogena dufluorido
- Nitrogena trifluorido
- Nitrogena unufluorido
- Nitrozila fluorido
- Tionila fluorido
- Trifluoroacetata acido
Vidu ankaŭ
[redakti | redakti fonton]- Kemio
- Listo de kemiaj elementoj laŭ nomo
- Listo de kemiaj elementoj laŭ simbolo
- Listo de kemiaj elementoj laŭ atomnumero
Eksteraj ligiloj
[redakti | redakti fonton]- http://www.webelements.com/webelements/elements/text/F/index.html pri fluoro
- http://education.jlab.org/itselemental/ele009.html pri fluoro
- http://www.chemie-master.de/pse/pse.php?modul=F pri fluoro
Referencoj
[redakti | redakti fonton]- ↑ (angle): Atomic weights of the elements 2013 (IUPAC Technical Report) (PDF), p. 8
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||