Fosfora pentafluorido
Aspekto
(Alidirektita el Fosfora kvinfluorido)
| Fosfora pentafluorido | ||||
 | ||||
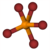
| Plata kemia strukturo de la Fosfora pentafluorido | ||||
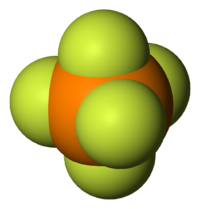 | ||||
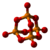
| Tridimensia kemia strukturo de la Fosfora pentafluorido | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 7647-19-0 | |||
| ChemSpider kodo | 22715 | |||
| PubChem-kodo | 24295 | |||
| Merck Index | 15,7464 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora, nebrulema, koroda, termo-stabila, fumiganta gaso kun malagrabla penetranta odoro | |||
| Molmaso | 125,966 g·mol−1 | |||
| Denseco | 5,527g cm−3 | |||
| Fandpunkto | −93,8 °C | |||
| Bolpunkto | −75 °C | |||
| Ekflama temperaturo | −84,6 °C[1] | |||
| Solvebleco | Akvo:reakcias | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R26 R35 [2] | |||
| Sekureco | S9 S26 S36/37/39 S45 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H280, H314, H330 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P271, P280, P284, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P320, P321, P363, P403+233, P405, P410+403, P501[3] | |||
(25 °C kaj 100 kPa) | ||||
Fosfora pentafluorido aŭ PF5 estas neorganika kombinaĵo de fosforo kaj fluoro, senkolora, nebrulema, koroda, termo-stabila, fumiganta gaso kun malagrabla penetranta odoro, uzata kiel potenca, oksidiga kaj fluorigagento en kemiaj sintezoj. Fosfora pentafluorido estis malkovrita en jaro 1876 de la brita kemiisto Thomas Edward Thorpe (1845-1925), verkinto de ia Historio pri kemio (1910).[4]
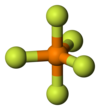
| Struktura simileco | |||
|

| ||
| Pro la simileco de molekulaj strukturoj, silicia tetrafluorido, fosfora pentafluorido kaj sulfura heksafluorido estas alte volatilaj substancoj.[5] | |||
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per reakcio inter fosfora pentaklorido kaj arsena trifluorido:[6]
Sintezo 2
[redakti | redakti fonton]- Per interagado de fosfora pentaklorido kaj "kalcia fluorido":
Sintezo 3
[redakti | redakti fonton]- Per traktado de fosfora pentaklorido kun fluorida acido:
Sintezo 4
[redakti | redakti fonton]- Per reakcio inter fosfora pentaklorido kaj zinka fluorido:
Sintezo 5
[redakti | redakti fonton]- Per interagado de fosfora pentaklorido kun natria fluorido:
Sintezo 6
[redakti | redakti fonton]- Metodo de Henri Moissan (1852-1907) kreita en 1886: Reakcio inter fosfora trifluorido kaj bromo formante la adukton fosfora trifluoro-dubromido. Poste, per malkomponado la antaŭa komponaĵo iĝas en fosfora pentafluorido kaj fosfora pentabromido:
Sintezo 7
[redakti | redakti fonton]- Per malkomponado de fosfora trifluorido:
Sintezo 8
[redakti | redakti fonton]- Per traktado de fosfora trifluorido kun fluoro:
Sintezo 9
[redakti | redakti fonton]- Per agado de sulfura trioksido sur fosforila fluorido kaj fluorida acido:
Sintezo 10
[redakti | redakti fonton]- Per agado de fosforila fluorido sur natria fluorido:
Sintezo 11
[redakti | redakti fonton]- Per interagado de nitrila fluorido kaj fosfino:
Sintezo 12
[redakti | redakti fonton]- Per traktado de fosfora pentaoksido kun kalcia fluorido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Malkomponado de fosfora pentafluorido:
Reakcio 2
[redakti | redakti fonton]- Hidrolizo per formado de fosforila fluorido kaj fluorida acido:
Reakcio 3
[redakti | redakti fonton]- Kiam hidrolizo okazas per eksceso da akvo fosfata acido estiĝas:
Reakcio 4
[redakti | redakti fonton]- Reakcio de fosfora pentafluorido kun natria hidroksido:
Reakcio 5
[redakti | redakti fonton]- Reakcio de fosfora pentafluorido kun silicia oksido:
Reakcio 6
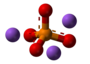
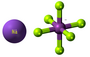
[redakti | redakti fonton]- Preparado de kompleksaĵo natria fosfora-heksafluorido:
Reakcio 7
[redakti | redakti fonton]- Nitroniuma heksafluoro-fosfato estiĝas per reakcio inter fosfora pentafluorido, nitrata acido kaj klorida acido:[7]
Reakcio 8
[redakti | redakti fonton]- Sintezo de fluorometano per interagado de fosfora pentafluorido kaj metanolo:
Reakcio 9
[redakti | redakti fonton]- Preparado de difluorofosfata acido per agado de fosfora pentaflorido kaj sulfuro en akva medio:
Reakcio 10
[redakti | redakti fonton]- Preparado de litia heksafluoro-fasfato per traktado de fosfora pentafluorido kaj litia fluorido:[8]
Reakcio 11
[redakti | redakti fonton]- Sintezo de natria heksafluorofosfato per agado de fosfora pentafluorido kaj natria hidroksido:
Reakcio 12
[redakti | redakti fonton]- Sintezo de silicia kvarfluorido per traktado de fosfora pentafluorido kaj silicia tetraoksido en akva medio:
Literaturo
[redakti | redakti fonton]- Cameo Chemicals
- Advances in Hydrofluoric Acid Research and Application
- Lithium Compounds—Advances in Research and Application
- Across Conventional Lines
- Pharmacology of Fluorides
- The Chemistry of Fluorine







![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)


![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{300^{o}C=400^{o}C}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8e723954705252c3fd86edc7d999e0ae101b2a0c)