Valento (kemio)
En kemio, la valento de elemento estas mezuro de ĝia kombinivo kun aliaj atomoj kiam ĝi formas molekulojn. La koncepto de valento estis evoluigita en la dua duono de la 19a jarcento kaj sukcesis klarigi la molekulan strukturon de neorganikaj kaj organikaj kombinaĵoj.[1] La serĉo por la fundamentoj de valento kondukis al la modernaj teorioj de kemia ligado, inkluzive de la kuba atomo (1902), sed poste malakceptita, Lewis-strukturoj (1916), valenta ligada teorio (1927), molekulaj orbitaloj (1928), teorio pri valentŝela elektronpara forpelado (1958) kaj ĉiuj altnivelaj metodoj de kvantuma kemio.
Priskribo[redakti | redakti fonton]
La kombivo de atomo estas kalkulebla de la nombro da hidrogenaj atomoj kun kiuj ĝi kombiniĝas En metano, karbono havas valenton 4; en amoniako, nitrogeno havas valenton 3; en akvo, oksigeno havas valenton 2; kaj en hidrogena klorido, kloro havas valenton 1. Kloro, ĉar ĝi havas valenton 1, estas anstataŭigebla por hidrogeno, do forsforo havas valenton 5 en forsfora pentaklorido, PCl5. Valentaj skemoj de kombinaĵo simboligas la konekteblecon de la elementoj, kun linioj desegnitaj inter du elementoj, foje nomitaj ligoj, simboligas saturitan valenton por ĉiu elemento.[1] Ekzemploj estas:
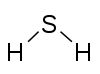
| Kombinaĵo | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
|---|---|---|---|---|---|---|---|---|---|
| Skemo | 
|

|

|
|

|

| |||
| Valencies | Hidrogeno, 1 | Karbono 4, Hidrogeno 1
|
Karbono 4, Hidrogeno 1
|
Karbono 4, Hidrogeno 1
|
Nitrogeno 3, Hidrogeno 1
|
Natrio 1, Karbono 4, Nitrogeno 3
|
Sulfuro 2, Hidrogeno 1
|
Sulfuro 6, Oksigeno 2, Hidrogeno 1
|
Kloro 7, Oksigeno 2
|
Valento priskribas nur konekteblecon; ĝi ne priskribas la geometrion de molekulaj kombinaĵoj aŭ kio estas nun sciata esti jonaj kombinaĵoj aŭ gigantaj kovalentaj strukturoj. Linio inter atomoj ne simboligas elektronparon kiel en Lewis skemoj.
Modernaj difinoj[redakti | redakti fonton]
Valento estas difinita de la IUTAK jene:[2]
- La maksimuma nombro da unuvalentaj atomoj (originale hidrogenaj aŭ kloraj atomoj) kiuj povas kombiniĝi kun atomo de la konsiderata elemento aŭ kun fragmento aŭ por kiu atomo de ĉi tiu elemento povas esti anstataŭigita.
Alternativa moderna priskribo estas:[3]
- La nombro da hidrogenaj atomoj kiuj povas kombiniĝi kun elemento en binara hidrido aŭ dufoje la nombro da oksigenaj atomoj kombiniĝanta kun la elemento en ĝia oksido aŭ oksidoj.
Ĉi tiu difino malsamas al la IUTAK-difino ĉar oni povas diri ke elemento povas havi pli ol unu valenton.
Historia evoluado[redakti | redakti fonton]
La vorto "valento" venas de la latina vorto valentia "forto, kapablo", de pli frua vorto valor "valoro" kaj la kemia signifo, kiu rilatas al la "kombinivo de elemento", aperis en 1884, kiel la germana vorto Valenz.[4]

En 1789, William Higgins eldonis bildojn, kiuj antaŭsignis la koncepton de valentaj ligoj.[5] Se, ekzemple, laŭ Higgins, la forto inter la baza partiklo de oksigeno kaj la baza partiklo de nitrogeno estis 6, tiam la forto estus dividita laŭe, kaj same por la aliaj kombinaĵoj de bazaj partikloj (vidu la ilustraĵon).
La iniciato, tamen, de la teorio de kemia valento estas spurita al 1852-a referaĵo de Edward Frankland, en kiu li kombinis la pli malnovajn teoriojn de liberaj radikaloj kaj “tipoteorio” kun pensoj pri kemia afineco por montri ke certaj elementoj emas kombini kun aliaj elementoj por formi kombinaĵojn kiuj enhavas 3, t.e., en la 3-atomaj grupoj (ekz., NO3, NH3, NI3, ktp.) aŭ 5, t.e., en la 5-atomaj grupoj (ekz., NO5, NH4O, PO5, ktp.), ekvivalentojn de la ligitaj elementoj. Tiel, laŭ Frankland, iliaj afinacioj estas plejbone plenumeblaj. Sekve de ĉi tiuj ekzemploj kaj postulatoj, Frankland deklaris kiom evidenta ĝi estas ke[6]
- Tendenco aŭ leĝo regas (ĉi tie), kaj tion, kio ajn estas la kvalito de la kombiniĝantaj atomoj, la kombinivo de la alloganta elemento, se mi rajtas uzi tiun terminon, ĉiam kontentigas la sama nombro da tiuj atomoj.
Tiun “kombinivon” oni poste nomis kvantovalento aŭ valento.[5] En 1857 August Kekulé proponis konstantajn valentojn por multaj elementoj, ekzemple 4 por karbono, kaj uzis ilin proponante strukturajn formulojn por multaj organikaj molekuloj, kiuj estas ankoraŭ akceptataj.
Plejmultaj 19a-jarcentaj kemiistoj difinis la valenton de elemento kiel la nombro da ĝiaj ligoj sen distingi malsamajn tipojn de valento aŭ ligo. Tamen, en 1893 Alfred Werner priskribis transirmetalajn kunordiĝajn kompleksojn, ekzemple [Co(NH3)6]Cl3, en kiu li distingis unuarangan kaj duarangan valentojn, rilatajn al la modernaj konceptoj de oksidiĝa stato kaj kunordiĝa nombro respektive.
Por ĉefgrupaj elementoj, en 1904 Richard Abegg konsideris pozitivan kaj negativan valentojn (maksimuman kaj minimuman oksidiĝan staton) kaj proponis regulon kiu diris ke ilia diferenco estas ofte 8.
Elektronoj kaj valento[redakti | redakti fonton]
La Rutherford-modelo de la kernohava atomo (1911) montris ke la ekstero de atomo estas okupita de elektronoj, kiu sugestas ke elektronoj kaŭzas la interagojn de atomoj kaj la formadon de kemiaj ligoj. En 1916, Gilbert N. Lewis klarigis valenton kaj kemian ligadon laŭ emo de (ĉefgrupaj) atomoj atingi stabilan okopon de valentoŝelaj elektronoj. Laŭ Lewis, kovalenta ligado kondukas al okopoj de kunhavataj elektronoj kaj jona ligado kondukas al okopoj per translokigo de elektrono(j) de unu atomo al la alia. La termino kovalento estas atribuita al Irving Langmuir, kiu deklaris en 1919 ke "la nombro da paroj de elektronoj kiujn donita atomo kunhavas kun la apudaj atomoj estas la kovalento de tiu atomo".[7] La prefikso ko- signifas "kune", do kovalenta ligo signifas ke la atomoj kunhavas valenton. Nuntempe, oni kutime parolas pri kovalenta ligo prefere ol "valento", pro la antaŭenigoj en la teorio de kemia ligado, sed estas ankoraŭ ĝenerale uzata en elementaj studoj, kie ĝi provizas heŭristikan enkondukon al la temo.
En la 1930aj jaroj, Linus Pauling proponis ke ankaŭ ekzistas polaraj kovalentaj ligoj, kiuj estas mezaj inter kovalentaj kaj jonaj kaj ke la grado de jona kvalito dependas de la diferenco de elektronegativeco de la du ligitaj atomoj.
Pauling ankaŭ konsideris hipervalentajn molekulojn, en kiuj ĉefgrupaj elementoj ŝajne havas valenton pli grandan ol la maksimumo 4 permesita de la okopa regulo. Ekzemple, en la sulfura heksafluorida molekulo (SF6), Pauling konsideris ke la sulfuro formas 6 verajn du-elektronajn ligojn uzante tiel nomatajn sp3d2 hibridajn atomajn orbitalojn, kiuj kombinas unu s, tri p kaj du d-orbitalojn. Tamen poste, kvantummekanikaj kalkuloj pri tiu kaj similaj molekuloj montris ke la rolo de d-orbitaloj en la ligado estas minimuma kaj ke la SF6 molekulo devus esti priskribita kiel havanta 6 polarajn kovalentajn (parte jonajn) ligojn faritajn el nur kvar orbitaloj ĉe sulfuro (unu s kaj tri p) en akordo kun la okopa regulo, kune kun ses orbitaloj ĉe la fluoroj.[8] Similaj kalkuloj pri transirmetalaj molekuloj montras ke la rolo de p-orbitaloj estas negrava, do unu s kaj kvin d-orbitaloj ĉe la metalo estas sufiĉaj priskribi la ligadon.[9]
Oftaj valentoj[redakti | redakti fonton]
Por elementoj en la ĉefaj grupoj de la perioda tablo, la valento povas varii inter 1 kaj 7.
| Grupo | valento 1 | valento 2 | valento 3 | valento 4 | valento 5 | valento 6 | valento 7 | Tipaj valentoj |
|---|---|---|---|---|---|---|---|---|
| 1 (I) | NaCl | 1 | ||||||
| 2 (II) | MgCl2 | 2 | ||||||
| 13 (III) | BCl3, AlCl3 Al2O3 |
3 | ||||||
| 14 (IV) | CO | CH4 | 4 | |||||
| 15 (V) | NO | NH3 PH3 As2O3 |
NO2 | N2O5 PCl5 |
3 kaj 5 | |||
| 16 (VI) | H2O H2S |
SO2 | SO3 | 2 kaj 6 | ||||
| 17 (VII) | HCl | ClO2 | Cl2O7 | 1 kaj 7 |
Multaj elementoj havas kutiman valenton rilatitan al sia pozicio en la perioda tabelo kaj nuntempe tion raciigas la okopa regulo. La latinaj/grekaj prefiksoj uni-/mono-, bi-/di-, ter-/tri-, quadri-/tetra-, quinque-/penta- estas uzataj priskribi jonojn en la ŝargaj statoj 1, 2, 3, 4, 5 respektive. Plurvalenta aŭ multivalenta rilatas al specio kiu ne estas limigita al specifa nombro da valentaj ligoj. Specio kun unuobla ŝargo estas unuvalenta (monovalenta). Ekzemple, la Cs+ katjono estas unuvalenta katjono, dum la Ca2+ katjono estas duvalenta katjono kaj la Fe3+ katjono estas trivalenta katjono. Diference al Cs kaj Ca, Fe povas ankaŭ ekzisti en aliaj ŝargaj statoj, precipe 2+ kaj 4+ kaj estas tial konata kiel plurvalenta jono.[Citaĵo bezonata]
Komparo de valento kaj oksidiĝa stato[redakti | redakti fonton]
Pro la ambigueco de la termino valento, nuntempe aliaj notacioj estas uzataj en praktiko.[10] Krom la sistemo de oksidiĝaj nombroj kiel uzata en Stock-nomenklaturo por kunordigaj kombinaĵoj kaj la lambda-notacio, kiel uzata en la IUTAK nomenklaturo de neorganika kemio, oksidiĝa stato estas pli klara indiko de la elektronika stato de atomoj en molekulo.[11][12]
La oksidiĝa stato de atomo en molekulo donas la nombron da valentaj elektronoj kiujn ĝi akiris aŭ perdis.[13] En kontrasto al la valento, la oksidiĝa stato povas esti pozitiva (por elektropozitiva atomo) aŭ negativa (por elektronegativa atomo).
Elementoj en alta oksidiĝa stato povas havi valenton pli altan ol kvar. Ekzemple, en perkloratoj, kloro havas sep valentajn ligojn kaj rutenio, en la oksidiĝa stato +8 en rutenio tetroksido, havas ok valentajn ligojn.
Ekzemploj[redakti | redakti fonton]
(Valentoj laŭ la difino de nombro da valento ligado rilataj oksidiĝaj statoj)
| KOMBINAĴO | FORMULO | VALENTO | OKSIDIĜA STATO |
|---|---|---|---|
| Hidrogena klorido | HCl | H = 1 Cl = 1 | H = +1 Cl = −1 |
| Perklorata acido * | HClO4 | H = 1 Cl = 7 O = 2 | H = +1 Cl = +7 O = −2 |
| Natria hidrido | NaH | Na = 1 H = 1 | Na = +1 H = −1 |
| Fera (II) oksido ** | FeO | Fe = 2 O = 2 | Fe = +2 O = −2 |
| Fera (III) oksido ** | Fe2O3 | Fe = 3 O = 2 | Fe = + 3 O = −2 |
* La unuvalenta perklorata jono (ClO4−) havas valenton 1.
** Fera(II) oksido aperas en kristala strukturo, do ne eblas identigi tipan molekulon.
En fera(II) oksido, Fe havas oksidiĝan nombron II, en fera(III) oksido, oksidiĝan nombron III.
Ekzemploj kies valentoj kaj oksidiĝaj statoj malsamas pro ligoj inter identaj atomoj:
| KOMBINAĴO | FORMULO | VALENTO | OKSIDIĜA STATO |
|---|---|---|---|
| Kloro | Cl2 | Cl = 1 | Cl = 0 |
| Hidrogena peroksido | H2O2 | H = 1 O = 2 | H = +1 O = −1 |
| Etino | C2H2 | C = 4 H = 1 | C = −1 H = +1 |
| Hidrarga(I) klorido | Hg2Cl2 | Hg = 2 Cl = 1 | Hg = +1 Cl = −1 |
Valentoj ankaŭ povas esti malsamaj al absolutaj valoroj de oksidiĝaj statoj pro malsama polareco de ligoj. Ekzemple, en diklorometano, CH2Cl2, karbono havas valenton 4 sed oksidiĝan staton 0.
Difino de "Maksimuma nombro da ligoj"[redakti | redakti fonton]
Frankland opiniis ke la valento (li uzis la terminon "atomeco") de elemento estis ununura valoro kiu rilatas al la maksimuma valoro observebla. La nombro da neuzitaj valentoj ĉe atomo de kio estas nun nomita la p-blokaj elementoj estas ĝenerale para kaj Frankland sugestis ke la neuzitaj valentoj saturas unu la aliajn. Ekzemple, nitrogeno havas maksimuman valenton 5. Formante amoniakon du valentoj estas lasitaj neligitaj; sulfuro havas maksimuman valenton 6, formante hidrogenan sulfidon kvar valentoj estas lasitaj neligitaj.[14][15]
La Internacia Unio de Teoria kaj Aplika Kemio (IUTAK) plurfoje provis atingi sendubasencan difinon de valento. La nuna versio, adoptita en 1994:[16]
- La maksimuma nombro da unuvalentaj atomoj (originale hidrogenaj aŭ kloraj atomoj) kiuj povas kombiniĝi kun atomo de la elemento konsiderata aŭ kun fragmento aŭ por kiu atomo de ĉi tiu elemento povas esti anstataŭigita.[2]
Hidrogeno kaj kloro estis originale uzitaj kiel ekzemploj de unuvalentaj atomoj, pro ilia kvalito formi nur unu unuoblan ligon. Hidrogeno havas nur unu valentan elektronon kaj povas formi nur unu ligon kun atomo kiu havas nekompletan eksteran ŝelon. Kloro havas sep valentajn elektronojn kaj povas formi nur unu ligon kun atomo kiu donacas valentan elektronon kompletigi eksteran ŝelon de kloro. Tamen, kloro ankaŭ povas havi oksidiĝajn statojn +1 al +7 kaj povas formi pli ol unu ligon donacante valentajn elektronojn.
Kvankam hidrogeno havas nur unu valentan elektronon, ĝi povas formi ligojn kun pli ol unu atomo.
En la hidrofluorida jono ([HF2]−), ekzemple, ĝi formas tri-centran kvar-elektronan ligon kun du fluoridaj atomoj:
- [ F–H F– ↔ F– H–F ]
Alia ekzemplo estas la tri-centra du-elektrona ligo en diborane (B2H6).
Maksimumaj valentoj de la elementoj[redakti | redakti fonton]
Maksimumaj valentoj por la elementoj estas bazitaj sur la datumoj de listo de oksidiĝaj statoj de la elementoj.
Referencoj[redakti | redakti fonton]
- ↑ 1,0 1,1 Partington, James Riddick. (1921) A text-book of inorganic chemistry for university students, 1‑a eldono.
- ↑ 2,0 2,1 IUPAC Gold Book definition: valento
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997).
- ↑ Harper, Douglas. "valento" Arkivigite je 2015-12-22 per la retarkivo Wayback Machine.
- ↑ 5,0 5,1 Partington, J.R.. (1989) A Short History of Chemistry. Dover Publications, Inc. ISBN 0-486-65977-1.
- ↑ Frankland, E. (1852).
- ↑ (1919) “The Arrangement of Electrons in Atoms and Molecules”, Journal of the American Chemical Society 41 (6), p. 868–934. doi:10.1021/ja02227a002.
- ↑ E. Magnusson.
- ↑ (May 2014) “Chapter 7: Chemical bonding in Transition Metal Compounds”, The Chemical Bond: Chemical Bonding Across the Periodic Table. Wiley -VCH. ISBN 978-3-527-33315-8.
- ↑ The Free Dictionary: valento
- ↑ IUPAC, Gold Book definition: oxidation number
- ↑ IUPAC, Gold Book definition: lambda
- ↑ IUPAC Gold Book definition: oxidation state
- ↑ Frankland, E.. (1870) Lecture notes for chemical students(Google eBook), 2‑a eldono, J. Van Voorst.
- ↑ Frankland, E.. (1885) Inorganic chemistry, 1‑a eldono, p. 75–85.
- ↑ (1994) “Glossary of terms used in physical organic chemistry (IUPAC Recommendations 1994)”, Pure and Applied Chemistry 66 (5). doi:10.1351/pac199466051077.
Vidu ankaŭ[redakti | redakti fonton]
Eksteraj ligiloj[redakti | redakti fonton]
- esperante Nyilasi, János (1984) Molekuloj, Scienca Eldona Centro, Budapesto, Hungario, tradukis Kovács Lajos.
