Precipitado (kemio)
En kemio precipitado estas la kreo de solido. Kiam la reakcio okazas en likva solvaĵo, la solido formita estas la 'precipitaĵo'. La kemiaĵo kiu kaŭzas la reakcion estas la 'precipitanto'. Sen sufiĉa forto de gravito (sinkado) kunigi la partiklojn, la precipitaĵo restas kiel suspensiaĵo. Post sedimentiĝo, precipe uzante centrifugilon sinkigi ĝin en kompaktan amason, la precipitaĵon oni povas nomi 'buleto'. La likvaĵo restanta super la solido estas la 'superstaranta' solvaĵo.
Ofte la formado de precipitaĵo indikas la okazon de kemia reakcio. Se oni verŝas solvaĵon de arĝenta nitrato en solvaĵon de natria klorido, kemia reakcio okazas formante blankan precipitaĵon de arĝenta klorido. Kiam solvaĵo de kalia jodato reagas kun solvaĵo de plumba (II) nitrato, formiĝas flava precipitaĵo de plumba jodato.
Precipitado povas okazi se la koncentriĝo de solvitaĵo preterpasas ĝian solveblecon (ekzemple, miksante solvantojn aŭ ŝanĝante ilian temperaturon). Precipitado povas okazi rapide el supersaturita solvaĵo.
En solidoj, precipitado okazas se la koncentriĝo de unu solido estas super la solvebleca limo en la gastiganta solido, ekzemple rapidhardado aŭ jonenplantado kaj la temperaturo estas sufiĉe alta por ke difuzo apartigu en precipitaĵojn. Precipitado en solidoj estas rutine uzata por sintezi nanoakumuliĝojn.[1]
Grava stadio de la precipita procezo estas la komenciĝo de nukleiĝo. La kreo de hipoteza solida partiklo inkluzivas la formadon de interfaco, kiu postulas ioman energion bazitan sur la relativa surfaca energio de la solido kaj la solvaĵo. Se ĉi tiu energio ne estas havebla kaj taŭga nukleiĝa surfaco ne estas havebla, supersaturiĝo okazas.
Aplikoj[redakti | redakti fonton]


Precipitaj reakcioj estas utilaj por produkti pigmentojn, forigi salojn el akvo en akvopurigado, kaj en klasika kvalita neorganika analizo.
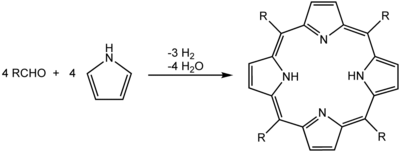
Precipitado estas ankaŭ utila por izoli la produktojn de reakcio dum sintezado. Ideale, la produkto de la reakcio estu nesolvebla en la reakcia solvanto. Tiel, ĝi precipitiĝas dum ĝi formiĝas, prefere formante purajn kristalojn. Ekzemplo tia estas la sintezo de porfirinoj en refluanta propionata acido. Malvarmigante la reakcian miksaĵon al ĉambra temperaturo, kristaloj de la porfirino precipitas kaj kolektiĝas per filtrado:[2]
Precipitado ankaŭ povas okazi kiam oni enmetas antisolvanton (solvanton en kiu la produkto estas nesolvebla), treege reduktante la solveblecon de la dezirita produkto. Poste, estas facile apartigi la precipitaĵon per filtrado, dekantado aŭ centrifugado). Ekzemplo estas la sintezo de kromika tetrafenilporfirina klorido: oni aldonas akvon al la DMF-solvaĵo kaj la produkto precipitiĝas.[3] Precipitado estas ankaŭ utila por purigi produktojn: oni solvas krudan bmim-Cl en acetonitrilo kaj verŝas ĝin en etilan acetaton, kie ĝi precipitiĝas.[4] Alia grava apliko de antisolvanto estas precipitiĝo de DNA per aldono de etanolo.
En metalurgio, precipitado el solida solvaĵo estas utila metodo plifortigi alojojn; ĉi tiu procezo estas konata kiel solid-solvaĵa plifortigo.
Bildigi per kemiaj ekvacioj[redakti | redakti fonton]
Ekzemplo de precipita reakcio: arĝenta nitrato (AgNO3) en akvo aldoniĝas al solvaĵo enhavanta kalian kloridon (KCl), kaj oni observas la precipitaĵon de blanka solido, arĝenta klorido (AgCl). (Zumdahl, 2005)
- AgNO3 (aq) + KCl (aq) → AgCl (s) + KNO3 (aq)
Ĉi tiu reago esti skribebla por emfazi la disociitajn jonojn en kombinita solvaĵo. Ĉi tiu nomiĝas jona ekvacio.
- Ag+ (aq) + NO3− (aq) + K+ (aq) + Cl− (aq) → AgCl (s) + K+ (aq) + NO3− (aq)
Alia metodo prezenti precipitan reakcion estas per neta jona reakcio. En ĉi tiu okazo, eventualaj spektantaj jonoj (kiuj ne kontribuas al la reakcio) estas ellasitaj el la formulo. Tio simpligas la suprajn ekvaciojn al la sekvanta:
- Ag+ (aq) + Cl− (aq) → AgCl (s)
Koloroj de precipitaĵoj[redakti | redakti fonton]
Multaj kombinaĵoj enhavantaj metalajn jonojn produktas precipitaĵojn kun distingaj koloroj. La jenaj estas tipaj koloroj por diversaj metaloj. Tamen, multaj de ĉi tiuj kombinaĵoj povas produkti kolorojn tre malsamajn ol tiuj listigitaj.
| Oro | Oranĝa |
| Kromo | Profunde verda, neklare verda, oranĝa, purpura, flava, bruna |
| Kobalto | Rozkolora |
| Kupro | Blua |
| Fero (II) | Verda |
| Fero (III) | Ruĝete bruna |
| Mangano | Palroza |
| Nikelo | Verda |
Plejmultaj kombinaĵoj formas blankajn precipitaĵojn.
Anjona-Katjona analizo[redakti | redakti fonton]
Precipitaĵa formado estas utila por distingi la tipon de katjono en salo. Por fari tion, alkalo unue reakcias kun la nekonata salo produkti precipitaĵon kiu estas la hidroksido de la nekonata salo. Por identigi la katjonon, oni notas la koloron de la precipitaĵo kaj ĝian solveblecon en eksceso. Similaj procezoj estas ofte uzataj en sinsekvo - ekzemple, solvaĵo de baria nitrato reakcias kun sulfataj jonoj formi solidan barian sulfaton, indikante ke probable ĉeestas sulfataj jonoj.
Digestado[redakti | redakti fonton]
Digestado aŭ maturiĝo de la precipitaĵo, okazas kiam ĵus formita precipitaĵo estas lasita, kutime ĉe pli alta temperaturo, en la solvaĵo el kiu ĝi precipitiĝis. Rezultas pli puraj kaj pli grandaj partikloj. La fizika-kemia procezo sur kiu baziĝas digestado estas nomita Ostwald-maturiĝo.
Vidu ankaŭ[redakti | redakti fonton]
Referencoj[redakti | redakti fonton]
- ↑ (2007) “Formation, Dynamics, and Characterization of Nanostructures by Ion Beam Irradiation”, Critical Reviews in Solid State and Materials Sciences 32 (1), p. 1–50. doi:10.1080/10408430601187624.
- ↑ A. D. Adler; F. R. Longo; J. D. Finarelli; J. Goldmacher; J. Assour; L. Korsakoff (1967). “A simplified synthesis for meso-tetraphenylporphine”, J. Org. Chem. 32 (2), p. 476–476. doi:10.1021/jo01288a053.
- ↑ Alan D. Adler; Frederick R. Longo; Frank Kampas; Jean Kim (1970). “On the preparation of metalloporphyrins”, Journal of Inorganic and Nuclear Chemistry 32 (7), p. 2443. doi:10.1016/0022-1902(70)80535-8.
- ↑ Dupont, J., Consorti, C., Suarez, P., de Souza, R. (2004).
Literaturo[redakti | redakti fonton]
- Zumdahl, Steven S.. (2005) Chemical Principles, 5‑a eldono, New York: Houghton Mifflin. ISBN 0-618-37206-7.
Zumdahl, Steven S.. (2005) Chemical Principles, 5‑a eldono, New York: Houghton Mifflin. ISBN 0-618-37206-7.
- Smith, Mark. (1993) Principles of Science.