Sulfurila fluorido
| Sulfurila fluorido | |||||
 | |||||
| Plata kemia strukturo de la Sulfurila fluorido | |||||
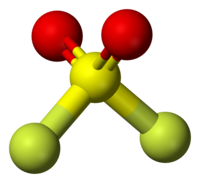 | |||||
| Tridimensia kemia strukturo de la Sulfurila fluorido | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 2699-79-8 | ||||
| ChemSpider kodo | 16647 | ||||
| PubChem-kodo | 17607 | ||||
| Merck Index | 15,9111 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora, senodora, toksa, irita, koroda gaso | ||||
| Molmaso | 102,055 g·mol-1 | ||||
| Denseco | 1,35g cm−3 | ||||
| Fandpunkto | -135,8°C | ||||
| Bolpunkto | -55,4°C | ||||
| Ekflama temperaturo | Nebrulema | ||||
| Solvebleco | Akvo:solvebla | ||||
| Mortiga dozo (LD50) | 100 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R23/25 R36/37/38 R50 R48/20 R23 | ||||
| Sekureco | S23 S37/39 S45 S61 S60/63 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H280, H330, H331, H370, H373, H400 | ||||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P270, P271, P273, P284, P304+340, P310, P311, P314, P320, P321, P391, P403+233, P405, P410+403, P501[1] | ||||
(25 °C kaj 100 kPa) | |||||
Sulfurila fluorido aŭ SO2F2 estas neorganika fluora komponaĵo de sulfuro kaj oksigeno, senkolora, senodora, penetranta, toksa, koroda, facile kondensigebla gaso kun proprecoj pli similaj al sulfura heksafluorido ol sulfurila klorido, estante rezista al hidrolizo eĉ supre de 150°C. Ĝi estas neŭrotoksa kaj potenca forceja gaso, sed vaste uzata kiel fumigilo kaj insekticido por kontrolado de termitoj, musoj kaj pestoj en agrikulturo. Sulfurila fluorido estas solvebla en akvo, kaj en ordinaraj organikaj solvantoj tiaj kiaj etanolo, tolueno kaj karbona kvarklorido.
La originala produkto estis patentigita en 1959 de la usona Dow Kompanio kiel pesticido por uzo en agrikulturo. Inhalado de sulfurila fluorido estas sandamaĝa kaj povas rezulti en spiririton, pulmedemon, naŭzon, stomakdoloron, deprimon de la centro nervoza sistemo, ŝveligon en la ekstremaĵoj, muskolajn kuntiriĝojn, konvulsiojn kaj morton. Ĉi-ekspozicioj okazas tiam kiam homoj eniras en neleĝaj strukturoj dum fumigado kun nesufiĉa aerumado. Epidemiologaj esploroj elmontris, ke fumigistoj uzantaj sulfurilan fluoridon prezentas neŭrologiajn efikojn, inklude de reduktita plenumado en kognaj provoj kaj normalaj memorkapablaj provoj krom reduktita flarfunkcio.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per traktado de sulfura duoksido sur fluoro:
Sintezo 2
[redakti | redakti fonton]- Per varma malkomponado de baria fluorosulfonato:
Sintezo 3
[redakti | redakti fonton]- Per interagado de metila fluorosulfinato kaj fluoro:
Sintezo 4
[redakti | redakti fonton]- Per traktado de sulfurila klorido fluorido kun kalia fluorosulfinato:
Sintezo 5
[redakti | redakti fonton]- Per traktado de sulfura duoksido kun arĝenta (II) fluorido:
Sintezo 6
[redakti | redakti fonton]- Per traktado de sulfurila klorido kun natria fluorido:
Sintezo 7
[redakti | redakti fonton]- Per reakcio inter baria klorido kaj fluorosulfonata acido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Malkomponado de sulfurila fluorido:
Reakcio 2
[redakti | redakti fonton]- Hidrolizo de sulfurila fluorido:
Reakcio 3
[redakti | redakti fonton]- Preparado de natria fluorosulfonato:
Reakcio 4
[redakti | redakti fonton]- Preparado de sulfamido:
Reakcio 5
[redakti | redakti fonton]- Sintezo de fenil-fluorosulfonato:
Vidu ankaŭ
[redakti | redakti fonton]- Sulfurila klorido
- Sulfurila bromido
- Sulfurila jodido
- Tionila fluorido
- Tionila klorido
- Tionila bromido
- Tionila jodido
Literaturo
[redakti | redakti fonton]- National Pesticide Information Center
- Chemical Book
- California Department of Pesticide Regulation[rompita ligilo]
- Pesticide Residues in Food
- Report 2005
- Handbook of Pesticide Toxicology: Principles and Agents








![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)





