Tioacetata acido
Etoso
| Tioacetata acido | |||||
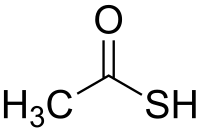
| |||||
| Plata kemia strukturo de la Tioacetata acido | |||||

| |||||
| Tridimensia strukturo de la Tioacetata acido | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 507-09-5 | ||||
| ChemSpider kodo | 10052 | ||||
| PubChem-kodo | 10484 | ||||
| Merck Index | 15,9473 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora ĝis flaveca koloro kun akra malagrabla odoro. | ||||
| Molmaso | 76.11756 g·mol−1 | ||||
| Denseco | 1.075 g cm−3 | ||||
| Fandpunkto | −17 °C | ||||
| Bolpunkto | 97 °C | ||||
| Refrakta indico | 1,4648 | ||||
| Ekflama temperaturo | 18 °C | ||||
| Memsparka temperaturo | forte hidrolizas ĉe alta temperaturo | ||||
| Solvebleco | Akvo:
| ||||
| Mortiga dozo (LD50) | 75 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Risko | R11 R22 R34 R43 | ||||
| Sekureco | S9 S16 S26 S36/37/39 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj[1] | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H225, H301, H302, H314, H317, H318 | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P272, P280, P301+310, P301+312, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P310, P321, P330, P333+313, P363, P370+378, P403+235, P405, P501 | ||||
(25 °C kaj 100 kPa) | |||||
Tioacetata acido estas organosulfura komponaĵo, flaveca likvaĵo kun forte malagrabla odoro, ĝenerale uzata en organikaj sintezoj por enkonduko de la tiolaj grupoj en molekuloj. Saloj de la tioacetata acido uzatas por generado de tioacetataj esteroj.
Tioacetata acido uzatas en sintezoj de organikaj komponaĵoj, malmoliga agento por rezinoj, retigagentoj, metalurgio, pesticidoj, farmaciaĵoj kaj kiel larmigiloj. Tioloj estas pli fortaj acidoj ol alkoholoj kaj fenoloj. Tioloj kun hidrogena peroksido produktas sulfoksidojn[2] kaj sulfonojn.
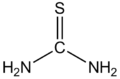
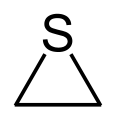
| Bonvolu ne konfuzi... | |
 |
 |
| Ambaŭ estas izomeroj kaj ambaŭ estas organikaj acidoj, sed la unua enhavas tiometanatan grupon ligitan al metila radikalo kaj la dua prezentas metanatan kaj merkaptanan grupojn ambaŭ ligitajn al metilena grupo. | |
Sintezoj
[redakti | redakti fonton]- August Kekulé sintezis la tioacetatan acidon per varma interagado de la acetata acido kun la fosfora kvinsulfido.[3]
10 CH3COOH + 2 P2S5 → 10 CH3COSH + 2 P2O5
- Alternative, tioacetata acido povas esti preparata per traktado de la acetata anhidrido kaj la sulfida acido[3]:
C4H6O3 + H2S → C2H4OS + C2H4O2
- Tioacetatan acidon estigas etil-tioacetato per agado sur etileno:
C2H2 + C2H4OS → C2H4OS + C2H4O2
- Laŭ la metodo de Edward kaj Wong, hidratigo de la tioacetanilido estigas anilinon kaj tioacetata acido.[4]

Literaturo
[redakti | redakti fonton]- Chemical Book
- Chemicalland21
- Science Lab[rompita ligilo]
- Cameo Chemicals
- Office of Radiation, Chemical & Biological Safety [rompita ligilo]
- Science of Synthesis: Houben-Weyl Methods of Molecular Transformations Vol ..., Andre B. Charette
- Advances in Enzymology and Related Areas of Molecular Biology, Volume 11, Alton Meister
Kunrilataj kemiaĵoj
[redakti | redakti fonton]-
Etanotiolo -
Propanotiolo -
Tiirano -
Tiireno -
Tietano -
Tieteno -
Tiolano
Vidu ankaŭ
[redakti | redakti fonton]Referencoj
[redakti | redakti fonton]- ↑ PubChem
- ↑ Sulfoksido estas kemia komponaĵo enhanvanta iun sulfinilan (SO) funkcian grupon ligita al du karbonatomoj.
- ↑ 3,0 3,1 The Development of Modern Chemistry, Aaron J. Ihde
- ↑ Organic Chemistry, Part 1 of 3, Richard Daley