Tirozolo
| Tirozolo | ||
 | ||
| Plata kemia strukturo de la Tirozolo | ||
 | ||
| Tridimensia kemia strukturo de la Tirozolo | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 501-94-0 | |
| ChemSpider kodo | 9964 | |
| PubChem-kodo | 10393 | |
| Merck Index | 15,10022 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka solidaĵo | |
| Molmaso | 138,164 g·mol−1 | |
| Denseco | 1,0742g cm−3[1] | |
| Fandpunkto | 91 °C | |
| Bolpunkto | 375,2 °C[2] | |
| Refrakta indico | 1,5590 | |
| Ekflama temperaturo | 143,2 °C[3] | |
| Acideco (pKa) | 10,17 | |
| Solvebleco | Akvo:124 g/L | |
| Sekurecaj Indikoj | ||
| Riskoj | R20 R21 R36/37/39 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501[4] | |
(25 °C kaj 100 kPa) | ||
Tirozolo aŭ C8H10O2 estas feniletanoida kunmetaĵo prezentanta fenolan radikalon ligitan en la 4-a pozicio de la benzena ringo al etanola radikalo. Ĝi estas la plej grava reprezentanto en la Oliv-oleo kie ĝi okazas nature aŭ sub la estera formo. Tirozolo estas senkolora solidaĵo sub media temperaturo kaj solvebla en akvo, etanolo, acetono, duetila etero kaj acetata acido.
Ĝi posedas antioksidigajn proprecojn kaj povas protekti la ĉelojn kontraŭ la oksidiva streso. Ĝi estas abunde trovata en naturo kaj en la blanka vino, kaj ankaŭ estas korprotektaĵo. Kvankam ĝi ne estas tiel potenca kiel aliaj oksidigantoj en la olivoleo kiel la "oleuropeino" kaj la "oleokantalo", ĝi tamen estas vaste uzata en la mediteranea dieto kaj plenumas signifan rolon por la sano kaj la bonaj rezultoj de ĉi tiu dieto.
Laŭ nuntempaj eksperimentoj en la Universitato de Pizo kaj Universitato de Milano, oni konstatis ke la tirozolo sendube influas pozitivmaniere sur la ĉelojn per ĝia antioksidiga agado kaj abrupte malaltigas la ekaperon de inflamigaj procezoj kiuj kondukas al produktado de la ostoporozo aŭ reŭmatoida artrito.
Ĝia derivaĵo, la hidroksotirozolo, posedas antimikrobiajn proprecojn. Laŭ multaj raportoj, la hidroksotirozolo estas la plej grava biofenolo en la olivoleo simila al la fenolaj komponaĵoj trovataj en la verda teo kaj en la ruĝa vino.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]Sintezo 2
[redakti | redakti fonton]- Preparado ekde la "hidrokso-tirozolo":
Sintezo 3
[redakti | redakti fonton]- Preparado ekde la fenetila alkoholo:
Sintezo 4
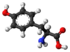
[redakti | redakti fonton]- Biologia konvertado ekde la fenilalanino. Per senkarboksiligo oni estigas la fenetilaminon. Per aldono de akvo-molekulo oni forigas la amoniakon. Trie, por aldoni hidroksilon en la 4-a pozicio de la aromata ringo, oni reakciigas kun bromo kaj poste natria hidroksido:
Sintezo 5
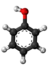
[redakti | redakti fonton]- Preparado ekde la fenolo kaj "kloroetanolo":
Sintezo 6
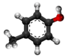
[redakti | redakti fonton]- Preparado ekde la "p-krezolo" kaj "klorometanolo":
Sintezo 7
[redakti | redakti fonton]- Preparado ekde la "p-klorofenolo" kaj etanolo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Konvertado al tirozino:
Reakcio 2
[redakti | redakti fonton]- Konvertado al "hidrokso-tirozolo":
Reakcio 3
[redakti | redakti fonton]- Konvertado al fenetila alkoholo:
Reakcio 4
[redakti | redakti fonton]- Konvertado al fenilalanino:
Reakcio 5
[redakti | redakti fonton]Reakcio 6
[redakti | redakti fonton]- Konvertado al "p-krezolo" kaj "klorometanolo":
Literaturo
[redakti | redakti fonton]- Science Direct
- NCBI Resources
- YMDB
- ResearchGate
- DBPedia
- Semantic Scholar
- Olive Oil: Minor Constituents and Health
- New Look to Phytomedicine: Advancements in Herbal Products as Novel Drug Leads




![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f7bf1d1bb277e0c1c24fb38c4d34882382b8e4bf)
![{\displaystyle {\mathsf {{\xrightarrow[{-NH_{3}}]{+H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f4aabba41606e113cf208763408d08710dc56adf)
![{\displaystyle {\mathsf {{\xrightarrow[{-H_{2}O}]{LiAlH_{4}\,[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c5edf195a795148e1adbf26bfa76c9e21435088e)
![{\displaystyle {\mathsf {{\xrightarrow[{+NaOH\,-\,NaBr}]{+Br_{2}\,-HBr}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/64b8610979c915011a79fca30794d02343b32f47)

![{\displaystyle {\mathsf {{\xrightarrow[{+OH}]{+H_{2}O\,-NH_{3}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/abec186af99fef1db0b988f40eadfcd7879449a0)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-HCl}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/354bdf82974c03eebc473b62fc780fef4b52eb01)



![{\displaystyle {\mathsf {{\xrightarrow[{+NH_{2}Cl\,-HCl}]{+CO}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/64fe8484b2341fe5f332425e1d2654622b666c97)
![{\displaystyle {\mathsf {{\xrightarrow[{+NH_{2}Cl\,-HCl}]{+CO\,+H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/80215df10343b631b52b8059d5f064b48bb9c468)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)
![{\displaystyle {\mathsf {{\xrightarrow[{LiAlH_{4}}]{+Cl_{2}\,-HCl}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/393d04bb131fde05efe0c98f4d96b7915c47ee1d)