Karviono
| Karviono | |||

| |||
| Kemia strukturo | |||
| |||
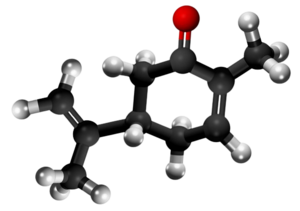
| 3D Kemia strukturo | |||

| |||
| Mentha longifolia | |||

| |||
| Semoj de Anethum graveolens. | |||
| Alternativa(j) nomo(j) | |||
| Karvolo | |||
| Kemia formulo | |||
| CAS-numero-kodo | |||
| ChemSpider kodo | |||
| Fizikaj proprecoj | |||
| Aspekto | Klara, senkolora kaj palflava likvaĵoj | ||
| Molmaso | 150.22 g mol−1 | ||
| Smiles |
| ||
| Denseco | 0.96 g/cm3 (likva) | ||
| Refrakta indico | 1,4970 | ||
| Fandopunkto | 25.2 °C (77.4 ℉; 298.3 K) | ||
| Bolpunkto | 231 °C (448 ℉; 504 K) (91 °C 5 mmHg) | ||
| Solvebleco | Akvo: (malvarma) nesolvebla
| ||
| Solvebleco | Etanolo: solvebla
| ||
| Mortiga dozo (LD50) | 3562 mg/kg | ||
| Ekflama temperaturo | 98 °C (208.4 ℉) | ||
| Sekurecaj Indikoj | |||
| Risko | R22 | ||
| Sekureco | |||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[1][2] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H302, H313, H316, H317 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P270, P272, P280, P301+312, P302+352, P321, P330, P333+313, P363, P501 | ||
(25 °C kaj 100 kPa) | |||
Karviono estas natura substanco apartenanta al la familio de la terpenoidoj, trovata en multaj esencoleoj, tamen, ĝi estas pli abunda en la semoj de la Carum carvi kaj Anethum graveolens. Karviono formas du reflektajn bildojn aŭ enantiomerojn: R-(–)-karviono kaj S-(+)-karviono[3], kiu posedas odoron de karvio-semoj.
La fakto ke la du enantiomeroj estas percepteblaj pro iliaj malsimilaj flaroj elmontras ke la olfataj akceptantoj devas enteni kiralajn grupojn, permesante ke ili identigu unu enantiomeron pli forte ol la alia. Ne ĉiuj enantiomeroj posedas distingeblajn odorojn. Oni ankaŭ malkovris ke la sajmirienoj kapablas distingi la enantiomerojn de la karviono.
Okazejo
[redakti | redakti fonton]La S-(+)-karviono estas la ĉefa konstituanto (60%-70%) en la esencoleoj de karvio, kiu estas larĝaskale produktita ĉirkaŭ 10 tunoj/jare. Ĝi same okazas koncentrita ĉirkaŭ 40%-60% en la semoleo de la aneto, kaj ankaŭ en la oranĝoŝela oleo de la mandarinujo. R-(–)-karviono estas ankaŭ la plej abunda komponaĵo en la esencoleo de pluraj specioj de mento, aparte la mentoleo de la Mentha spicata, kiu komponiĝas inter 50%-80% da R-(–)-karviono, kaj estas la ĉefa fonto de tiu enantiomero.
Tamen, la plejmulto el la R-(–)-karvionoj uzataj en komercaj aplikaĵoj estas sintezita ekde la R-(+)-limoneno. La izomero de la R-(–)-karviono same okazas en la kuromojoleo[4][5]. Kelkaj oleoj, samkiel la oleo de la Cymbopogon martinii enhavas miksaĵojn da ambaŭajn enantiomerojn. Multaj aliaj naturaj oleoj, ekzemple la pipromentoleo enhavas etajn kvantojn da karvionoj.
Historio
[redakti | redakti fonton]La karvio estis uzata por medicinaj celoj de la antikvaj romianoj, sed la karviono, kvankam ĝi estis unue studita de la germana kemiisto Schweizer, kiu nomis ĝin karvolo (ĉar li kredis ke ĝi estas alkoholo), ĝi estis nur izolita en ties natura formo far la kemiisto Franz Varrentrapp (1815-1877) en 1849. Goldschmidt kaj Zűrrer ĝin identigis ĝin kiel ketono rilatita al la limoneno, kaj la strukturo estis finfine klarigita far Jegor Vagner, en 1894.
Preparado
[redakti | redakti fonton]La dekstro-forma S-(+)-karviono estis produktita praktike pura per frakcia distilado de la karvioleo. La levo-forma enantiomero estis produktita el la oleoj kiuj enhavas ĝin kaj ĝenerale ĝi bezonas aldonan traktadon por produktado de la R-(−)-karviono kun alta pureco.
Ĉi-tio oni atingas per formiĝo de aldona kombinaĵo kun la Sulfida acido, el kiu la karviono estas regenerita per traktado kun kalia hidroksido en etanolo kun posta distiliĝo de la produkto sub vaporkurento.Karviono estas sinteze preparebla elde la limoneno pere de la "limonena nitrozoklorido", kiu estiĝas per traktado de la limoneno kun "izoamila nitrito" en glacia acetata acido. Ĉi-komponaĵo estas konvertita al karbokzimo, kiu povas estiĝi per refluo kun dumetil-formamido aŭ DMF en izopropanolo.
La refluo de la karvokzimo kun 5% da okzalata acido produktas karvionon. Ĉi-tiu procezo estigas R-(−)-karvionon el la R-(+)-limoneno. La plej granda uzo de la d-limoneno estas kiel antaŭanto de la S-(+)-karviono. La larĝaskala disponebleco de oranĝoŝeloj, iu flanka produkto en la industrio de oranĝosuko, igas la limonenon malaltkoste disponebla, kaj la kunresponda sinteza karviono malaltkoste preparita.
Izomeroj de la karviono
[redakti | redakti fonton]-
Krizantenono -
Levoverbenono -
Mentofurano -
Perilaldehido -
Perileno -
Rozofurano -
Umbelulono -
Verbenono
Literaturo
[redakti | redakti fonton]- Handbook on Oleoresin and Pine Chemicals (Rosin, Terpene Derivatives, Tall ...[rompita ligilo], H. Panda
- Natural Extracts Using Supercritical Carbon Dioxide, Mamata Mukhopadhyay
- Flavours and Fragrances: Chemistry, Bioprocessing and Sustainability, Ralf Günter Berger
- Plant Drug Analysis: A Thin Layer Chromatography Atlas, Sabine Bladt, Eva M. Zgainski
- The Utilization of Bioremediation to Reduce Soil Contamination: Problems and ..., Václav Sasek, John A. Glaser, P. Baveye
- Introduction to Organic Laboratory Techniques: A Small Scale Approach, Donald L. Pavia
- Fenaroli's Handbook of Flavor Ingredients, Fifth Edition, George A. Burdock
- The terpenes
- Henriette's book
- Hindawi
- Experimental and Therapeutic Medicine
- The Dictionary of Substances and Their Effects: C, S. Gangolli
Vidu ankaŭ
[redakti | redakti fonton]-
Kariofileno -
Perilata alkoholo -
Verbenolo -
Verbenono
Referencoj
[redakti | redakti fonton]- ↑ Sigma Aldrich[rompita ligilo]
- ↑ PubChem
- ↑ La reprezentaĵoj R- kaj S- por enantiomeroj signifas la bildon reflektitan sur la spekulo en ĝiaj dekstra (R:rectus) kaj (S:sinister) maldekstra pozicioj. Kelkfoje la enatiomeroj estas ankaŭ reprezentataj de la literoj (L: laevo, levorotacia aŭ maldekstrorotacia) kaj (R: rectus, dekstrorotacia).
- ↑ Essential Oils Handbook Arkivigite je 2015-07-15 per la retarkivo Wayback Machine, H. Panda
- ↑ Pharmacognosy And Pharmacobiotechnology, Ashutosh Kar




























