Bajkaleino
| Bajkaleino | ||
 | ||
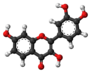
| Plata kemia strukturo de la Bajkaleino | ||
 | ||
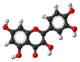
| Tridimensia kemia strukturo de la Bajkaleino | ||
 | ||
| Bajkaleino estas antioksidiga substanco kun antiinflamaj proprecoj trovata en plantoj de la familio de la Scutellaria baicalensis[1] | ||
| Kemia formulo | ||
| CAS-numero-kodo | 491-67-8 | |
| ChemSpider kodo | 4444924 | |
| PubChem-kodo | 5281605 | |
| Merck Index | 15,935 | |
| Fizikaj proprecoj | ||
| Aspekto | flava solidaĵo | |
| Molmaso | 270,240 g·mol-1 | |
| Denseco | 1,328g cm−3[2] | |
| Fandpunkto | 256°C-271°C[3] | |
| Bolpunkto | 650,2°C[4] | |
| Ekflama temperaturo | 225,3 °C | |
| Solvebleco | Akvo:0,1125 g/L [5] | |
| Sekurecaj Indikoj | ||
| Riskoj | R20/21/22 R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501[6] | |
(25 °C kaj 100 kPa) | ||
Bajkaleino, (5,6,7-trihidrokso-flavono) aŭ C15H10O5 estas organika kombinaĵo apartenanta al la familio de la flavonoloj, flava solidaĵo nesolvebla en akvo sed solvebla en metanolo, etanolo, duetila etero, acetono, etila acetato, glacia acetata acido kaj malmulte solvebla en kloroformo kaj nitrobenzeno.
Bajkaleino ĉeestas en la radikoj de la familio de la Scutellaria baicalensis kaj "Scutellaria lateriflora". Ĝi ankaŭ troviĝas en la rizomoj de la Oroxylum indicum kaj timianoj. Bajkaleino estas fitokemiaĵo kun sennombraj aktivecoj, tiaj kiaj antiinflamaj, antivirusaj kaj antitumoraj.
Krom tio, ĝi estas potenca antioksidigaĵo[7] kaj inhibas la lipidan peroksidadon en mitokondrioj. Eblaj antideprimivaj efikoj atribuiĝas al la bajkaleino en eksperimentoj faritaj kun bestoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado ekde la akacetino per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj aldono de metoksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 2
[redakti | redakti fonton]- Preparado ekde la apigenino per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 3
[redakti | redakti fonton]- Preparado ekde la fisetino per aldono de du hidroksilaj grupoj en la 5-a kaj 6-a pozicioj de la kromenonila grupo kaj forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 4
[redakti | redakti fonton]- Preparado ekde la kempferolo per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicio de la kromenonila grupo kaj forigo de hidroksila grupo en la 4-a pozicioj de la fenila grupo:
Sintezo 5
[redakti | redakti fonton]- Preparado ekde la kverketino per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupoj en la 3-a pozicio de la kromenonila grupo kaj forigo de du hidroksilaj grupoj en la 3-a kaj 4-a pozicioj de la fenila grupo:
Sintezo 6
[redakti | redakti fonton]- Preparado ekde la miriketino per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicioj de la kromenonila grupo kaj forigo de tri hidroksilaj grupoj en la 3-a, 4-a kaj 5-a pozicioj de la fenila grupo:
Sintezo 7
[redakti | redakti fonton]- Preparado ekde la naringenino per aldono de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Konvertado al akacetino per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj forigo de metoksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 2
[redakti | redakti fonton]- Konvertado al apigenino per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 3
[redakti | redakti fonton]- Konvertado al fisetino per forigo de du hidroksilaj grupoj en la 5-a kaj 6-a pozicioj de la kromenonila grupo kaj aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 4
[redakti | redakti fonton]- Konvertado al kempferolo per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicio de la kromenonila grupo kaj aldono de hidroksila grupo en la 4-a pozicioj de la fenila grupo:
Reakcio 5
[redakti | redakti fonton]- Konvertado al kverketino per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupoj en la 3-a pozicio de la kromenonila grupo kaj aldono de du hidroksilaj grupoj en la 3-a kaj 4-a pozicioj de la fenila grupo:
Reakcio 6
[redakti | redakti fonton]- Konvertado al miriketino per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicioj de la kromenonila grupo kaj aldono de tri hidroksilaj grupoj en la 3-a, 4-a kaj 5-a pozicioj de la fenila grupo:
Reakcio 7
[redakti | redakti fonton]- Konvertado al naringenino per forigo de hidroksila grupo en la 6-a pozicio de la kromenonila grupo kaj aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Literaturo
[redakti | redakti fonton]- Advances and Challenges in Nanomedicine
- Cancer Inhibitors from Chinese Natural Medicines
- Dietary Interventions in Liver Disease: Foods, Nutrients, and Dietary ...
- Science Direct
- Hindawi
- Examining the Development, Regulation, and Consumption of Functional Foods
- Bioactive Natural Products: Chemistry and Biology
- Dictionary of Nutraceuticals and Functional Foods




![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)