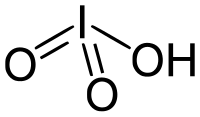
Jodata acido
| Jodata acido | ||||
| ||||

| ||||

| ||||
| Alternativa(j) nomo(j) | ||||
Jodato de hidrogeno
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 7782-68-5 | |||
| ChemSpider kodo | 22761 | |||
| PubChem-kodo | 24345 | |||
| Fizikaj proprecoj | ||||
| Aspekto | blanka solido, romba piezoelektra kristaloj | |||
| Molmaso | 175.91 g/mol g mol−1 | |||
| Smiles | O=I(=O)O | |||
| Denseco | 4.62 g/cm3 (likva) | |||
| Fandopunkto | 110 °C (230 ℉; 383 K) | |||
| Solvebleco:Akvo | 269 g/100 mL (20 °C) | |||
| Solvebleco | Nesolvebla en | |||
| Acideco (pKa) | 0.75 | |||
| Ekflama temperaturo | Ne bruliva | |||
| Sekurecaj Indikoj | ||||
| Risko | ||||
| Sekureco | ||||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS etikedigo de kemiaĵoj[1] | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Damaĝo | |||
| GHS Deklaroj pri damaĝoj | H272, H314 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P220, P221, P260, P264, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P370+378, P405, P501 | |||
(25 °C kaj 100 kPa) | ||||
Jodata acido aŭ HIO3 estas oksoacido de jodo, blanka solido, tre solvebla en akvo kaj ekzistanta en pura stato, kontraŭe al klorata acido kaj bromata acido, kiuj ekzistas nur en solvaĵoj. Jodata acido enhavas jodon kun oksidonombro +5 kaj estas unu el la plej stabilaj el la halogenidaj oksoacidoj en ties pura stato. Kiam zorge varmigita, la jodata acido malkomponiĝas en "joda kvinoksido" aŭ I2O5. Kun sinsekva varmigo, la joda kvinoksido plu malkomponiĝas estigante miksaĵon da jodo, oksigeno kaj jodoksidoj kun malpli altaj oksidonombroj.
Preparado[redakti | redakti fonton]
Jodata acido estas produktebla per oksidado de jodo kun fortaj oksidantoj, tiel kiel nitrata acido, kloro, klorata acido kaj hidrogena peroksido, ekzemple:
Proprecoj[redakti | redakti fonton]
Jodata acido estas relative forta acido kun (pKa) 0.75. Ĝi estas forta oksidanto en acida solvaĵo, sed malpli acida en baza solvaĵo. Kiam jodata acido aktivas kiel oksidanto, tiam la reakciprodukto estas aŭ jodo, aŭ joda jono.
Sub specialaj kondiĉoj (tre malalta pH kaj alta koncentriĝo de kloridjono [Cl−], ekzemple, en koncentrita klorida acido), jodata acido reduktiĝas al "joda triklorido" (ICl3), iu orflava komponaĵo en solvaĵo kaj nenia alia reduktiĝo okazas. En la foresto de la kloridjonoj, kiam ekzistas troo da reduktanto, tiam la tuta jodato (IO3−) konvertiĝas en jodidjono (I−).
Jodata acido uzatas kiel forta acido en analiza kemio. Ĝi eble uzatas por normigi solvaĵojn, kaj de malfortaj, kaj fortaj bazoj, uzante "metilruĝon" aŭ metiloranĝon kiel indikilon.
Jodata acido uzatas en la sintezo de natria aŭ kalia jodato, pro tio ke ĝi pliigas la jodenhavon de la salo.
Mineralaj acidoj[redakti | redakti fonton]
| Halogenidaj acidoj | |||||||
| HF | Fluorida acido | HCl | Klorida acido | HBr | Bromida acido | HI | Jodida acido |
| HFO | Hipofluorita acido | HClO | Hipoklorita acido | HBrO | Hipobromita acido | HIO | Hipojodita acido |
| HFO2 | Fluorita acido | HClO2 | Klorita acido | HBrO2 | Bromita acido | HIO2 | Jodita acido |
| HFO3 | Fluorata acido | HClO3 | Klorata acido | HBrO3 | Bromata acido | HIO3 | Jodata acido |
| HFO4 | Perfluorata acido | HClO4 | Perklorata acido | HbrO4 | Perbromata acido | HIO4 | Perjodata acido |
Literaturo[redakti | redakti fonton]
- Sigma-Aldrich[rompita ligilo]
- ACS Publications
- ACS Publications
- Chemical Book
- Concise Encyclopedia Chemistry, Mary Eagleson









