Linalila ftalato
Etoso
| Linalila ftalato | |||
 | |||
Linalila ftalato | |||
 | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| Fizikaj proprecoj | |||
| Molmaso | 438,608g mol−1 | ||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H360, H400 | ||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P273, P281, P308+313, P391, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
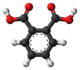
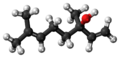
Dulinalila ftalato aŭ C28H38O4 estas kemia komponaĵo, apartenanta al la funkcia grupo de la esteroj de la ftalata acido kaj linalolo. Linalila ftalato estas kemia reakciaĵo, uzata en la fabrikado de ftalata acido derivaĵoj kaj linalilaj derivaĵoj. Linalila ftalato estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Linalila ftalato reakcias kun fortaj oksidigagentoj kaj fortaj bazoj kaj posedas antifungajn kaj antibakteriajn proprecojn.
Sintezoj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Preparado de linalila ftalato per interagado de ftalata acido kun linalolo:
Reakcio 2[redakti | redakti fonton]
- Preparado de linalila ftalato per interagado de ftalata anhidrido kun linalolo:
Reakcio 3[redakti | redakti fonton]
- Preparado de linalila ftalato per interagado de linalila klorido kun ftalata acido:
Reakcio 4[redakti | redakti fonton]
- Preparado de linalila ftalato per interagado de linalila klorido kun natria ftalato:



![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)





