Kvartionata acido
| Kvartionata acido | |||
| |||
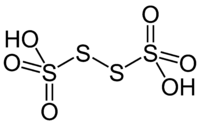
| Kemia strukturo de la Kvartionata acido | |||

| |||
| 3D Kemia strukturo de la Kvartionata acido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 13760-29-7 | ||
| ChemSpider kodo | 3846747 | ||
| PubChem-kodo | |||
| Fizikaj proprecoj | |||
| Aspekto | Senkolora solvaĵo | ||
| Molmaso | 226,27228 g mol−1 | ||
| Sekurecaj Indikoj | |||
| Risko | R36 R37 R38 | ||
| Sekureco | S26 S36 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Kvartionata acido, hidrogena kvartionato aŭ H2S4O6 estas okso-acido de sulfuro, kie du sulfuratomoj ĉeestantaj en la molekulo prezentas oksidonombron 0 kaj du +5. Aliflanke, la kombinaĵo povas esti konsiderata adukto rezultanta el ligaĵo inter iu bazo de Lewis S22− al SO3. Kvartionata acido apartenas al la familio de la politionataj acidoj kies membroj estas H2S2O6, H2S3O6, H2S5O6, krom aliaj.
Proprecoj[redakti | redakti fonton]
Ĝi estas dumero de la sulfata acido, formita per dusulfida ligaĵo. Ĉi-komponaĵo antaŭ longe uzatas por pludaŭrigi la koagulado-tempon kaj kiel antidoto en cianida venenigo. Kvartionata buljono estas blanka precipitaĵo kiu malpermesas la kreskon de gram-pozitivaj bakterioj, kaj la kvartionato estigita post aldono de solvaĵo de jodo aŭ jodido, inhibas la intestajn mikroorganismojn ĉeestantaj en la fekaj specimenoj.
La solvaĵoj de politionata kaj kvartionata acidoj estas sufiĉe stabilaj en altaj koncentriĝoj sen la ĉeesto de aero dum longaj periodoj. Maljunaj solvaĵoj malkomponiĝas al sulfata acido, sulfura duoksido kaj elementa sulfuro.
Sintezo[redakti | redakti fonton]
- Kvartionata acido estas oksidiga produkto de tiosulfato kun jodo:[1][2]
- Interagado de sulfida acido kaj sulfura trioksido:[3]
- Tiosulfata acido reakcias kun dutionita acido por doni kvartionatan acidon[4]
- Kiam tiosulfato oksidatas per milda oksidigagento tiel kiel ferika klorido aŭ kuprika salo, ĝi formas kvartionaton:[4]
- Reakcio kun kuprika klorido:[4]
Reakcioj[redakti | redakti fonton]
- Neŭtraliga reakcio de kvartionata acido kaj amoniako:
- Iom da tiosulfata acido reakcias kun kvartionata acido por doni kvintionatan acidon kaj sulfitan acidon:[4]
Literaturo[redakti | redakti fonton]
- Learn Chemistry
- NCBI Resources
- Sigma Aldrich
- Sulphur Atomistry
- Chemical Book
- PAN Pesticides Database - Chemicals
- Neogen.com Arkivigite je 2015-06-29 per la retarkivo Wayback Machine
Vidu ankaŭ[redakti | redakti fonton]
| ||||||
Referencoj[redakti | redakti fonton]
- ↑ The Chemical Gazette: Or, Journal of Practical Chemistry, in All ..., Volume 6, William Francis, Henry Croft
- ↑ Yumpu
- ↑ Sulphur atomistry
- ↑ 4,0 4,1 4,2 4,3 Inorganic Polymers. P. B. Saxena










