Metakrilata acido
| Metakrilata acido | |||
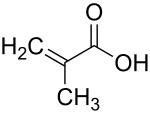 | |||
| Plata kemia strukturo de la Metakrilata acido | |||
 | |||
| Tridimensia strukturo de la Metakrilata acido | |||
 | |||
| Metakrilata acido trovatas en la folioj de la kamomilo | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 79-41-4 | ||
| ChemSpider kodo | 3951 | ||
| PubChem-kodo | 4093 | ||
| Merck Index | 15,6013 | ||
| Aspekto | senkolora solido aŭ likvaĵo kun akre malagrabla odoro | ||
| Fizikaj proprecoj | |||
| Molmaso | 86.06 g·mol−1 | ||
| Denseco | 1.015 g cm−3 | ||
| Fandpunkto | 15 °C | ||
| Bolpunkto | 161 °C | ||
| Refrakta indico | 1,4314 | ||
| Ekflama temperaturo | 77.2 °C | ||
| Memsparka temperaturo | 400 °C | ||
| Solvebleco | Akvo:9 g/100ml | ||
| Mortiga dozo (LD50) | 180 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Risko | R20/21/22 R35 R37 | ||
| Sekureco | S20/21/22 S26 S35 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H302+332, H311, H314, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P280, P305+351+338, P310 | ||
Metakrilata acido estas organika acida kombinaĵo, senkolora kaj viskozeca likvaĵo kun malagrabla odoro. Ĝi estas solvebla en varma akvo kaj mikseblas kun plejmulto el la organikaj solvantoj. Metakrilata acido industrie produktatas larĝaskale kiel antaŭanto de ĝiaj esteroj, ĉefe la metila metakrilato kaj ĝia polimero la polimetila metakrilato.
La metakrilatoj havas sennombrajn uzojn, plej specife en la manufakturo de polimeroj. La metila metakrilato nature okazas en etaj kvantoj en la oleo de la Chamaemelum nobile. Akrilata kaj metakrilata acidoj facile polimerizas en ĉeesto de lumo, varmo kaj oksigeno, kaj ankaŭ sub la agado de oksidigagentoj tiaj kiaj la peroksidoj. Ankaŭ ripetitaj frostoj kaj fandprocezoj povas kaŭzi polimerizon.
| Geometria Izomerio | |||
 |
 |

| |
Historio[redakti | redakti fonton]
Metakrilata acido estis unue sintezita de Edward Frankland (1825-1899)[1] kaj Baldwin Francis Duppa (1828-1873)[2] sub la formo de ĝia etila estero per reakcio kun fosfora kvinklorido kaj estero de izobuterata acido. En 1880, la polimera formo de la metakrilata acido estis unue priskribita. Ĝi nature okazas kiel estero de la kamomiloleo.
Sintezo[redakti | redakti fonton]
- La industria metodo por sintezado de la metakrilata acido kaj ĝiaj esteroj sidas sur la interagado de acetono-cianohidrino kaj akvo:

- Per oksidiga senhidrogenigo de la izobutirata acido:

- Per oksidado de la metakroleino en ĉeesto de molibdena, vanada kaj fosfora kataliziloj:[3]

- Per oksidado de la izobutileno kun nitrogena duoksido
- Per kataliza oksidado de la izobutileno kun atmosfera oksigeno tra la etapo de la metakroleina formiĝo.
Literaturo[redakti | redakti fonton]
- NIST Chemistry WebBook
- Cameo Chemicals
- Handbook of Fillers, Extenders, and Diluents, Michael Ash, Irene Ash
- Handbook of Rubber Bonding, Bryan G. Crowther
- Handbook of Commercial Catalysts: Heterogeneous Catalysts, Howard F. Rase
- Venomous Animals and Their Toxins, G. Habermehl
- Chemical Book
Kunrilataj kemiaĵoj[redakti | redakti fonton]
Vidu ankaŭ[redakti | redakti fonton]
Referencoj[redakti | redakti fonton]
- ↑ Edward Frankland: Chemistry, Controversy and Conspiracy in Victorian England, Colin A. Russell
- ↑ Journal of the Chemical Society
- ↑ 3,0 3,1 Polyoxometalate Molecular Science, Juan J. Borrás-Almenar, E. Coronado, Achim Müller, Michael Pope






