Dukloro-metano
| Duklorometano | |||
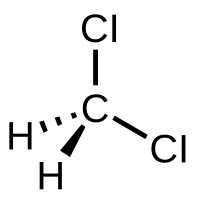 | |||
| Plata kemia strukturo de la Duklorometano | |||
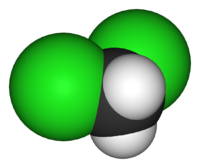 | |||
| Tridimensia kemia strukturo de la Duklorometano | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 75-09-2 | ||
| ChemSpider kodo | 6104 | ||
| PubChem-kodo | 6344 | ||
| Merck Index | 15,6135 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora, nebrulema, volatila likvaĵo | ||
| Molmaso | 84,927 g·mol-1 | ||
| Denseco | 1,3266g cm−3 | ||
| Fandpunkto | −96,7 °C | ||
| Bolpunkto | 39,6 °C | ||
| Refrakta indico | 1,4242 | ||
| Memsparka temperaturo | 556 °C | ||
| Solvebleco | Akvo:17,5 g/L | ||
| Mortiga dozo (LD50) | 1250 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R40 | ||
| Sekureco | S2 S23 S24/25 S36/37 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H302, H315, H319, H335, H336, H341, H351, H373 | ||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P280, P281, P301+312, P302+352, P304+340, P305+351+338, P308+313, P314, P321, P330, P332+313, P337+313, P362, P403+233, P405, P501[1] | ||
(25 °C kaj 100 kPa) | |||
Duklorometano aŭ Klorido de metileno (formulo CH2Cl2) estas klororgana komponaĵo, senkolora, nebrulema, volatila likvaĵo devenanta el metano, kie duhidrogenoj estis anstataŭitaj de du kloratomoj. Klorido de metileno havas iomete dolĉecan odoron kaj estas vaste uzata kiel solvanto. Kvankam ĝi estas polara substanco, ĝi ne estas solvebla en akvo, sed miksiĝas kun multaj organikaj solvantoj tiaj kiaj etila acetato, alkoholoj, heksanoj, benzeno, karbona kvarklorido, dietila etero kaj kloroformo.
Ĝi ankaŭ estas multe uzata kiel farbo-forigaĵo kaj sengrasigaĵo[2]. En nutro-industrio, ĝi uzatas kiel senkafeina kafo kaj teo samkiel en preparado-ekstraktoj de lupoloj kaj aliaj gustigaĵoj. Ĝia volatileco rezultis en ĝia uzo kiel aerosola sprajilo por ĵetpelaĵoj kaj kiel blovagento en la fabrikado de poliuretanaj ŝaŭmoj. Klorido de metileno jam estis uzata kiel inhala anestezilo kaj agas kiel narkotaĵo en altaj koncentriĝoj. Kiam varmigita ĝi eligas toksajn fumojn kune kun fosgeno.
Duklorometano estis unue priskribita de la franca kemiisto Henri Victor Regnault (1810–1878)[3], kiu izolis ĝin ekde miksaĵo da klorometano kaj kloro kiu estis ekspoziciita al sunlumo.
Klasata kiel neŭrotoksa, duklorometano povas kaŭzi damaĝojn al cerbo kaj al centra nervo sistemo. La usona Agentejo por Protektado al Vivmedio (EPA) klasigis ĝin kiel potence karcinomogena al homoj, ĉar altaj ekspozici-niveloj al tiu kemiaĵo estis konfirmitaj kiel kaŭzo pri kancero-kazoj en bestaj hepatoj kaj pulmoj.[4]
Nerostitaj kafofaboj estas vaporigitaj ripetitaj fojoj en duklorometano ĝis kompleta elĉerpiĝo de la kafeino. Sekve, la solvanto estas tute drenita lasante malantaŭe plengustajn kafofabojn, tamen sen la nekonvenaj substancoj.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
Sintezo 2[redakti | redakti fonton]
- Preparado per interagado de kloroformo, natria arsenito kaj natria hidroksido donante duklorometanon, natrian arsenaton tribazan kaj natrian bromidon:[5]
Sintezo 3[redakti | redakti fonton]
- Preparado per reakcio inter karbona kvarklorido kaj natria hidrido:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- En besta kaj homa organismoj, duklorometano metaboliĝas en CO, CO2, formiata acido kaj HCl. Tiuj reakcioj estis konstatataj en laboristoj ekspoziciataj al ĉi-tiu poluciaĵo:[6]
Reakcio 2[redakti | redakti fonton]
- Studoj faritaj in vitro en rataj hepatoj konstatis ke la citosolo konvertas duklorometanon en formaldehidon, kiu cetere estas karcinomagento:[6]
Literaturo[redakti | redakti fonton]
- Introduction to Organic Laboratory Techniques: A Small Scale Approach
- Organic Chemistry
- Land disposal, remedial action, incineration and treatment of hazardous waste
- Industrial Organic Chemicals
- Environmental Investigation and Remediation
- Synthetic Methods of Organometallic and Inorganic Chemistry







![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{400^{o}C-500^{o}C}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/55185ade769f52a3a1e9ba5efa611d7c3b775e6d)


![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)