Krizino
| Krizino | ||
 | ||
| Plata kemia strukturo de la Krizino | ||
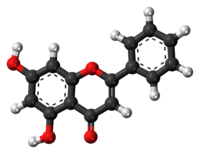 | ||
| Tridimensia kemia strukturo de la Krizino | ||
 | ||
| Krizino estas solida antioksidigaĵo trovata en plantoj tiaj kiaj la pasifloro[1] | ||
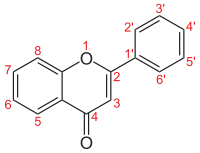 | ||
| Numerigo de la karbonaj strukturoj de la flavonoj. | ||
| Kemia formulo | ||
| CAS-numero-kodo | 480-40-0 | |
| ChemSpider kodo | 4444926 | |
| PubChem-kodo | 5281607 | |
| Fizikaj proprecoj | ||
| Aspekto | kristalflava solidaĵo | |
| Molmaso | 254,241 g·mol−1 | |
| Denseco | 1,2693g cm−3 | |
| Fandpunkto | 284 °C-286 °C[2] | |
| Bolpunkto | 491,9 °C[3] | |
| Refrakta indico | 1,6985 | |
| Ekflama temperaturo | 192,5 °C[4] | |
| Acideco (pKa) | 6,57 | |
| Solvebleco | Akvo:Nesolvebla | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Krizino, (5,7-duhidrokso-flavono) aŭ C15H10O4 estas flavonoido kun antioksidigaj proprecoj trovata en la mielo, propoliso, pasifloroj, Passiflora incarnata kaj "Oroxylum indicum". Ĝi estas kristalflava solidaĵo nesolvebla en akvo, solvebla en alkalaj solvaĵoj kaj malmulte solvebla en kloroformo, etanolo kaj duetila etero. Krizino posedas antimikrobiajn, antivirusajn, antifungajn, antimutagenajn kaj antikarcinomogenajn proprecojn krom vastan gamon da farmakologiaj aktivecoj. Samkiel aliaj flavonoidoj, krizino agas kontraŭ alergenoj, migrado de kancerĉeloj, kaj malpliigas la riskojn pri morteco en koronariaj kormalsanoj. Krizino estas uzatas en la traktado de la streso, ĝi estas antikonvulsia kaj provokas muskolan malstreĉiĝon.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado ekde la apigenino per forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 2[redakti | redakti fonton]
- Preparado ekde la luteolino per forigo de du hidroksilaj grupoj en la 4-a kaj 5-a pozicioj de la fenila grupo:
Sintezo 3[redakti | redakti fonton]
- Preparado ekde la naringenino per forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo kaj oksidado en la 2-a pozicio de la kromenonila grupo:
Sintezo 4[redakti | redakti fonton]
- Preparado ekde la miriketino per forigo de kvar hidroksilaj grupoj, nome tri en la 3-a, 4-a kaj 5-a pozicioj de la fenila grupo kaj unu en la 3-a pozicio de la kromenonila grupo:
Sintezo 5[redakti | redakti fonton]
- Preparado ekde la kempferolo per forigo de du hidroksilaj grupoj, unu en la 4-a pozicio de la fenila grupo kaj alia en la 3-a pozicio de la kromenonila grupo:
Sintezo 6[redakti | redakti fonton]
- Preparado ekde la kverketino per forigo de tri hidroksilaj grupoj, du en la 4-a kaj 5-a pozicioj de la fenila grupo kaj tria en la 3-a pozicio de la kromenonila grupo:
Sintezo 7[redakti | redakti fonton]
- Preparado ekde la akacetino per anstataŭado de metoksila grupo je hidrogenatomo en la 4-a pozicio de la fenila grupo:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Konvertado al apigenino per aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 2[redakti | redakti fonton]
- Konvertado al luteolino per aldono de du hidroksilaj grupoj en la 4-a kaj 5-a pozicioj de la fenila grupo:
Reakcio 3[redakti | redakti fonton]
- Konvertado al naringenino per aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo kaj reduktado en la 2-a pozicio de la kromenonila grupo:
Reakcio 4[redakti | redakti fonton]
- Konvertado al miriketino per aldono de kvar hidroksilaj grupoj, nome tri en la 3-a, 4-a kaj 5-a pozicioj de la fenila grupo kaj unu en la 3-a pozicio de la kromenonila grupo:
Reakcio 5[redakti | redakti fonton]
- Konvertado al "kempferolo" per aldono de du hidroksilaj grupoj, unu en la 4-a pozicio de la fenila grupo kaj alia en la 3-a pozicio de la kromenonila grupo:
Reakcio 6[redakti | redakti fonton]
- Konvertado al kverketino per aldono de tri hidroksilaj grupoj, du en la 4-a kaj 5-a pozicioj de la fenila grupo kaj tria en la 3-a pozicio de la kromenonila grupo:
Reakcio 7[redakti | redakti fonton]
- Konvertado al akacetino per anstataŭado de hidrogenatomo je metoksila grupo en la 4-a pozicio de la fenila grupo:
Literaturo[redakti | redakti fonton]
- Science Direct
- NCBI Resources
- Journal of endocrinology
- Nature
- Principles of Orthomolecularism
- Stopping the Clock
- A Dictionary of Chemistry and the Allied Branches ...
- Sleep and Sleep Disorders:: A Neuropsychopharmacological Approach





![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)



![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ee5440517c815e645f453d79ea37136e0c4ae6a6)




![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{+[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/dffae9f4f83c2c082f4d2260b0e74014e9e9594a)