Nitrilo
| Cianidoj aŭ nitriloj | |||||
 |
 |
 |
 |

| |
 |
 |
 |
 |

| |

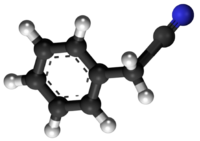
Nitrilo aŭ R-C≡N estas organika komponaĵo enhavanta la funkcian grupon cianidon aŭ C≡N. La prefikso ciano uzatas interŝanĝe kun la nitrila grupo en la industria literaturo. Nitriloj trovatas en pluraj utilaj kombinaĵoj, inklude de "metila cianoakrilato", uzata en super gluaĵoj, kaj "nitrila kaŭĉuko", ia polimero nitrilenhava uzata en laboratorioj kaj medicinaj gantoj. La nitrila kaŭĉuko ankaŭ uzatas kiel aŭtaj sigelringoj pro ĝia rezistemo al brulaĵoj kaj oleoj. Organikaj komponaĵoj enhavantaj multoblajn nitrilajn grupojn konatas kiel cianokarbonaĵoj[1].
Neorganikaj kombinaĵoj enhavanta la grupon cianon R-C≡N ne nomatas nitrilooj, sed cianidoj. Kvankam nitriloj kaj cianidoj povas deriviĝi el cianidaj saloj, la plejmulto el la nitriloj ne estas tiel toksaj. Industrie, la ĉefa metodo por produktado de nitriloj estas la amoniaka oksidado[2] kaj cianidigo[3]. Ambaŭ procezoj estas medisubteneblaj pro tio ke ili ne generas stekiometriajn kvantojn de saloj.
Historio[redakti | redakti fonton]
La vorto nitrilo estis unue uzita de Hermann Fehling (1811-1885), en 1844, en sia laboro pri la benzonitrilo. Tamen, la unua kombinaĵo de la homologa grupo de la nitriloj, la nitrilo de la formiata acido, tio estas, la hidrogena cianido estis unue sintezita de Carl Wilhelm Scheele (1742-1786), en 1782. En 1811, Gay-Lussac (1778-1850) sukcesis prepari la tre toksan kaj volatilan puran acidon. La nitrilo de la "benzoata acido" estis unue preparitaj de Friedrich Wöhler (1800-1882) kaj Justo de Libiko (1803-1873), sed, pro la minimuma sintezoproduktado nek la fizika kaj kemia proprecoj, nek la strukturo estis determinitaj. Teofilo Julio Peluzo (1807-1867) sintezis la "propanonitrilon", en 1834, kaj sugestis ke ĝi estis etero de la propanoata acido kun la hidrogena cianido. La sintezo de la benzonitrilo far Hermann Fehling, en 1844, per varmigo de amonia benzoato, estis la unua metodo kiu produktis sufiĉan substancon por la kemiaj eksperimentoj. Li determinis la strukturon per komparado de la jam konata sintezo de la hidrogena cianido, kaj varmigante amonian formiaton al ties reakciantoj. Li kojnis la vorton "nitrilon" por la ĵustrovita substanco, kaj ekde tiam ĝi fariĝis la nomon por ĉi tiu grupo da komponaĵoj.
Amoniaka oksidado[redakti | redakti fonton]
Laŭ ĉi-reakcio, unu hidrokarbonido estas parte oksidigita en la ĉeesto de la amoniako. Ĉi-konvertiĝo estas larĝaskale uzata en la produktado de la "akrilonitrilo".
En la produktado de la "akrilonitrilo", iu flanka produkto estas la "acetonitrilo". Multaj derivaĵoj el la benzonitrilo, ekzemple, la "ftalonitrilo", samkiel la "izobuteronitrilo" estas preparitaj per amoniaka oksidado. La procezo estas katalizita de metaloksidoj kaj supozeble la reakcio okazas pere de la aldehida vojo.
Cianida oksidado[redakti | redakti fonton]
Ĉi-metodo estas industria procezo por produktado de nitriloj ekde la hidrogena cianido kaj alkenoj. La procezo postulas homogenajn katalizilojn[4]. Ekzemplo de la cianidoksidado estas la produktado de "adiponitrilo", iu antaŭanto de la nilono 66[5] ekde la 1,3-butadueno:
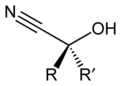
Cianohidrinoj[redakti | redakti fonton]
Cianohidrinoj estas speciala klaso da nitriloj kiuj rezultas el aldono de metalcianidoj al aldehidoj en la reakcio de la cianohidrinoj. Pro la polareco de la organika karbonilradikalo, ĉi reakcio ne postulas katalizilon, kontraŭe de la cianoksidigo de alkenoj. Ĝenerale, cianohidrinoj estas prepareblaj ekde dislokigo de sulfitoj per cianidaj saloj. Kutime, la cianohidrinoj estas perantoj en la aminoacidaj sintezoj de Strecker.
- Preparado de la laktonitrilo (iu cianhidrino) ekde interagado de la acetaldehido kaj natria sulfonato sekvata per cianigo de la natria 1-hidrokso-etanosulfonato:
Nitrilosintezo ekde senhidratigo de amidoj kaj okzimoj[redakti | redakti fonton]
Nitriloj povas prepariĝi per de senhidratigo de primaraj amidoj. Multaj reakciantoj estas disponeblaj, samkiel la kombinado de la "etiladuklorofosfato" kaj "1,8-duazaducikla-dekun-7-eno" laŭ la konvertiĝo de la benzamido al benzonitrilo.

Du perantoj en ĉi-reakcio estas la amida taŭtomero A kaj ties fosfatadukto[6] B
Preparado de nitriloj ekde organikaj halogenidoj kun cianidaj saloj[redakti | redakti fonton]
Ofte, nitriloj estas prepareblaj per vasta metodogamo. Ekzemple: la alkilaj halogenidoj[7] suferas nukleofilalifatan substituadon kun alkalometalaj cianidoj en la nitrilosintezo de Kolbe. Arilaj nitriloj estas prepareblaj laŭ la sintezo de Rosenmund-von Braun.
Per simila senhidratigo, sekundaraj amidoj estigas nitrilojn per "amida malkomponiĝo de von Braun". En ĉi-kazo, unu ligo C-N rompiĝas. La senhidratigo de la aldokzimo (RCH=NOH) same produktas nitrilojn. Tipaj reakciantoj por ĉi-transformiĝo estas "trimetilamino"/sulfura duoksido, zeolitoj aŭx "sulfurila klorido". Ekzemplo de ĉi-metodologio estas la sintezo de nitriloj ekde aldehidoj kun "hidroksilamino" en la ĉeesto de natria sulfato.

Nitrilaj sintezoj de Letts[redakti | redakti fonton]
La nitrilaj sintezoj de Letts estas kemia reakcio inter aromataj karboksilataj acidoj kun metalaj tiocianatoj por estigi nitrilojn. La reakcio inkludas perdon de karbona duoksido kaj "kalia hidrosulfido" aŭ KHS. Ĉi polarbaza substituo-reakcio estis malkovrita, en 1872, de Edmund Albert Letts (1851-1918).
Reakcio de Sandmeyer[redakti | redakti fonton]
Aromataj nitriloj ofte preparatas laboratorie ekde la anilino pere de "duazoniaj komponaĵoj". Ĉi-reakcio konatas kiel Reakcio de Sandmeyer, omaĝe al la svisa kemiisto Traugott Sandmeyer (1854-1922). La reakcio postulas transiĝon per metala cianido.

Aliaj metodoj[redakti | redakti fonton]
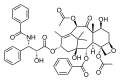
Komerca fonto por estigo de la cianida grupo estas la reakcio inter la "trietilaluminio" kaj la cianida acido por estigi la "duetilaluminian cianidon". Ĝi ofte uzatas en reakcioj de ketonoj kun nukleofila aldono, ekzemplo de tiu reakcio estas la totala sintezo de la taksolo far Kuvaĵima, omage al Isao Kuwajima[8].
La cianidaj jonoj faciligas la kupladon dubromidoj. La reakcio de la α,α'-dubroma adipata acido kun "natria cianido" en etanolo estigas la cianociklobutanon.

Laŭ la tiam-konata Reakcio de Franchimont (1872), unu el la α-bromokarboksilata acido[9] estas dumerizita[10] post hidrolizo de la cianogrupo kaj sekva senkarboksiligo[11].
Aromataj nitriloj estas prepareblaj ekde baza hidrolizo de la triklorometila arila ketimino (aŭ RC(CCl3)=NH) tiel kiel en la sintezo de Houben-fischer[12].
Nitroloj estas estigeblaj ekde primaraj aminoj per oksidado. La plej ordinaraj metodoj inkludas uzon de "kalia persulfato", trikloroizocianurata acido kaj anoda elektrosintezo[13].
α-aminoacidoj estigas nitrilojn kaj karbonan duoksidon per pluraj manieroj tra oksidiva senkarboksiligo[14].
Nitriloj[redakti | redakti fonton]
Vidu ankaŭ[redakti | redakti fonton]
-
Adiponitrilo -
Akrilonitrilo -
Aldokzimo -
Arila grupo -
Azo-bis-izo
buteronitrilo -
Benzamido -
Benzonitrilo -
Butadueno -
Cianohidrino -
Ciklobutano -
DBU -
Diazepam -
Duazometano -
Duazonia komponaĵo -
Ftalonitrilo -
Hidroksilamino -
Kalia persulfato -
Propanonitrilo -
Sulfurila klorido -
Taksolo -
Trietilaluminio -
Trietilamino -
Trikloro-izo
cianurata acido
Referencoj[redakti | redakti fonton]
- ↑ Cianokarbonaĵoj
- ↑ Amoniaka oksidado estas industria procezo por produktado de nitriloj uzante amoniakon kaj oksigenon.
- ↑ Cianidigo estas aldono de la jonoj H+ kaj CN- al iu molekula substanco.
- ↑ Homogena katalizilo estas miksaĵo da solveblaj kataliziloj.
- ↑ Nilono 66 estas tipo de poliamido: la plej ordinaraj poliamidoj estas la nilono 6 kaj la nilono 66.
- ↑ Adukto estas produkto de senpera aldono de du aŭ pli distingaj molekuloj, rezultante en ununuran reakciprodukton.
- ↑ Alkilaj halogenidoj estas grupo da kemiaj komponaĵoj derivitaj el alkanoj enhavanta unu aŭ pli da halogenidoj.
- ↑ The Story of Taxol: Nature and Politics in the Pursuit of an Anti-Cancer Drug, Jordan Goodman,Vivien Walsh
- ↑ Organic Chemistry Portal
- ↑ Dumero estas molekulo konsistanta el du ripetiĝantaj kemiaj radikoj.
- ↑ Senkarboksiligo estas perdo de la karboksilata radiko.
- ↑ Name Reactions and Reagents in Organic Synthesis, Bradford P. Mundy, Michael G. Ellerd, Frank G. Favaloro, Jr.
- ↑ Anoda elektrosintezo estas la sintezo de kemiaj komponaĵoj pere de iu elektrokemia ĉelo.
- ↑ Handbook of Vitamins, Third Edition, Robert B. Rucker, John W. Suttie, Donald B. McCormick
| ||||



![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)