Ŝtalo
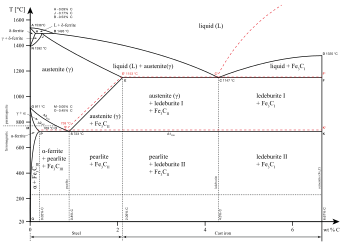
Fe3C = cementito; L = likvaĵo
Ŝtalo estas tre malmola metalo, alojo de fero kun kvanto da karbono inter 0,088% kaj 2,0%, la feraj alojoj kun pli ol 2.0% da karbono nomiĝas gisfero, tiaj alojoj estas tre fragilaj kaj ne eblas forĝi sed oni devas modligi ilin.
La ŝtalo ja estas forĝebla sen speciala traktado, kaj ĝi akireblas per traktadoj meĥanikaj aŭ varmaj diversajn ecojn. Malmola (dura) ŝtalo entenas inter 0,6 kaj 0,7 % da karbono, mola (maldura) ŝtalo entenas inter 0,15 kaj 0,25 % da karbono. La karakterizaĵoj de la ŝtalo dependas de la kvanton da alojaj elementoj kiun ĝi entenu. La ŝtaloj kiuj nure entenas karbonon nomiĝas karbonaj ŝtaloj.
La ŝtaloj kiuj entenas aliajn elementon ĥemian krom karbono estas nomataj de pluraj manieroj: Laŭ ĝia aplikado (Laborila ŝtalo), laŭ ĝia ĉefelemento/j aloja/j (Ekzemple, ŝtalo kiun entenu ĉefe mangano nomiĝas mangana ŝtalo, se ĝi entenas manganon kaj vanadon nomiĝos mangan-vanada ŝtalo, ktp) , laŭ specialaj karakterizaĵoj (rustorezista ŝtalo), laŭ la eblo de apliki specialan traktadon (nitrogenadebla ŝtalo), ktp. Je tre simpla maniero, oni povas nomi ordinaran ŝtalon al tiuj ŝtaloj kiuj nur entenas karbonon kaj ne havas specialan traktadon por modifi ĝian ecojn, al ĉiuj aliaj oni povas nomi kiel specialaj ŝtaloj.
Ĉefaj elementoj[redakti | redakti fonton]
La ŝtalo estas komponita ĉefe de du malsamaj elementoj: La fero kiu estas relative dura metalo, kaj la karbono estas nemetalo tre maldura en ĉiuj ĝiaj alotropaj statoj (Krom la diamanto, ambaŭ elementoj estas abundaj kaj facile akireblaj, tio faciligas la grand-skalan produktadon de ŝtalo.[1] Pro tio ĉi, la ŝtalo estas utilaj por pluraj uzoj kiel la kontruado de maŝinoj, laboriloj, konstruaĵoj ktp,. La ŝtalo kontribuas al teknologia disvolvado de la civilizacio.[2]
Malgraŭ ĝia alta denseco (7.850 kg/m³ komparita ekzemple kun la denseco de la aluminio: 2.700 kg/m³) la ŝtalo estas uzata en ĉiuj la industriaj sektoroj, eĉ en la aeronaŭtiko, ĉar la plej petataj pecoj devas esti tre eltenemaj.
Historio[redakti | redakti fonton]

A. Likva metalo B. Solidigita metalo C. Skorio D. Vandoj el kupro malvarmigita per akvo E. Fajrorezista materialo.
Oni ne konas la ekzaktan daton en kiu estis malkovrita la maniero por produkti feron per la fandado de mineraloj. Tamen, la unuaj arkeologiaj restaĵoj de iloj el fero datiĝas de ĉirkaŭ 3000 a.K.E kaj estis malkovritaj en Egiptujo. Kelkaj el la unuaj ŝtaloj venas el orienta Afriko, ĉirkaŭ 1400 a.K.E.[3] Dum la Dinastio Han en Ĉinio, oni produktis ŝtalon per la fandado de griza fero (gisfero) kun forĝa fero, ĉirkaŭ la 1-a jarcento a.K.E.[4] Ankaŭ ili adoptis la metodon por produkti wootz-ŝtalon, tiu metodo estas konita de la jaro 300 a.K.E en Barato kaj Srilanko, ĝi estis importita al Ĉinio je la 5-a jarcento. La wootz-ŝtalo estis eksportata al Mezoriento kaj tie oni el ĝi produktis la damaskan ŝtalon. Novaj reserĉadoj sugestis ke en la strukturo de la damaska ŝtalos estis karbonaj nanotuboj, kio klarigus kelkajn ecojn de la ŝtaloj - kiel ĝia forteco kaj elasteco - , kvankam pro la tiama teknologio, eblas ke la nanotuboj estu prodiktikaj hazarde kaj ne pro memvolo.[5]
Inter la 9-a kaj 10-a jarcento oni produktis en Merv krisol-ŝtalon. Oni produktis tiun ŝtalon varmigante kaj malvarmigante la feron kaj karbon per pluraj manieroj. Dum la Dinastio Song, inter la 11-a jarcento en Ĉinio, la produktado de ŝtalo estis farita per du manieroj: la unua produktis malaltkvalitan ŝtalon ĉar ĝi ne estis homogena, la dua maniero, antaŭanto de la Bessemer-metodo, forprenas la karbon per ripetataj forĝoj kaj malvarmigas rapide la pecon de ŝtalo.[6]
Ne ekzistas registro pri la konado de la Hardadebleco almenaŭ ĝis la mezepoko. La antikvaj metodoj por produkti ŝtalon estis produkti forĝan feron en forno, kun lignokarbo kaj blovante aeron al la forno, poste oni forpelis la ŝlakon per martelado, finfine oni karburiradis la forĝan ŝtalon por cementigi ĝin. Poste oni perfektigis la cementadon per la fandado de la cementita ŝtalon en krisoloj el argilo. Ĉe Sheffield (Anglujo), en 1740 oni produktis krisol-ŝtalon[2]. La metodo por produkti ĝin estis malkovrita de Benjamin Huntsman.

En 1856, Sir Henry Bessemer, kreis metodon por produkti ŝtalon grand-skale, tamen, ĉar oni nur povis uzi feron kun etaj kvanto da fosforo kaj sulfuro, la metodo ne estis tre utila kaj ĝi ne plu estis uzata.[7][8] Paul Héroult ekuzis elektr-arkajn fornojn por produkti ŝtalon grand-skale en 1902, li estis unu el la kreintoj de la nuna metodo por fandi aluminion. Per tiu metodo oni kreas elektran arkon per du karbonaj elektrodoj kiuj situas en la tegmento de la forno, la elektra arko fandas ŝtalan rubon kiu ĥemia komponado estas konata.
En 1948 oni inventis la metodon de "baza oksigeno (ankaŭ konata kiel la Linz-Donawitz-Verfahren-metodo aŭ la "oksigen-konvertada procezo"). Post la dua mondmilito pluraj landoj eksperimentiis kun pura oksigeno anstataŭ aero por plibonigi la metodon.
En 1950 oni inventis la "kontinuan fandadon", kiu estas procezo uzata kiam oni bezonas produkti grand-skale lamenigitajn profilojn el ŝtalo kies transversa sekco estas konstanta. La metodo konsistas en uzi moldilon kies formo estas tiu, kiu la ŝtalan pecon havos. La moldilo estas situanta sub krisolo, kiu kontrole permesas ke la fanda ŝtalo fluu al la moldilo. Per la gravito, la fanda materialo fluas moldilen, en la moldilo oni malvarmigas la fluaĵon per akvo-sistemo. Pro la malvarmigado la fluaĵon solidiĝas kaj adoptas la formon de la moldilo.
Nuntempe oni uzas kelkajn metalojn kaj metaloidojn, kiuj estas aldonataj al ŝtaloj por doni al ĝi durecon kaj aliajn ecojn.[9]
Tipoj[redakti | redakti fonton]
Laŭ Francisko Azorín ŝtalo estas Purigita fero, fandita kun malgranda kvanto da karbo.[10] Li indikas etimologion el la antikva germana stel, staklo (forta). Kaj li aldonas la jenajn tipoterminojn: Martina, Siemensa, cementita, fandŝtalo, gisita, krisola, pudla, nikela, tunstena.[11]
Produktado de ŝtalo[redakti | redakti fonton]
|
En la fazodiagramo fera-karbono (Fe-C)[12]) estas reprezentitaj la transformiĝoj, kiujn spertas la karbonaj ŝtaloj laŭ la temperaturo, ni konsideru ke la varmigado (aŭ malvarmigado) de la ŝtalo estas tre malrapida, tiel ke la difuz-procezo havas sufiĉe da tempo por finiĝi. Ĉi tiaj fazodiagramo estas akirita per eksperimentado. Dum la kreado de la fazodiagramo oni identigas la kritajn punktojn (t.e la specifaj temperaturoj en kiuj okazas la transformiĝoj) per pluraj manieroj.
Mikro-komponantoj[redakti | redakti fonton]
La pura fero havas tri alotropaj statoj kiuj aperas laŭ la plivarmigo de la temperaturo:
- De natur-media temperaturo ĝis 911 °C: La komuna fero, kristaliĝas en korpocentrita kuba krado kaj estas nomata kiel "ferito" aŭ "α-fero".[13] Ĝi estas duktila kaj fleksiĝema, ĝi permesas la bonan forĝadon de la alojoj kun malalta kvanto da karbono. La ferito estas feromagneta ĝis 768 °C (curie-temperaturo), je tiu temperaturo ĝi perdas tiun proprecon). La ferito akceptas tre malmulta kvanto da karbono.[13]
- Inter 911 kaj 1400 °C: La fero kristaliĝas en facocentrita kuba krado kaj estas nomata kiel "aŭstenito" aŭ "γ-fero". pro ĝia plialta kompakteco la aŭstenito estas pli facile deformebla. Ĝi estas paramagneta.
- Inter 1400 kaj 1538 °C: Ĝi denove kristaliĝas en korpocentra kuba kadro kaj estas nomata "δ-fero", kiu fakte estas la sama α-fero sed kun pligranda ret-parametro pro la temperaturo.
- Je plialtaj temperaturaj la fero troviĝas en likva stato.
Se oni aldonas karbonon al la fero, ĝiaj atomoj povus situi inter la spacoj de la kristalreto de la fero; tamen en la ŝtaloj la karbono kombinas kun la fero kaj produktas ferokarbidojn (Fe3C), t.e kemia komponaĵo kiu estas nomata kiel "cementito", do la karbonaj ŝtaloj estas komponataj de ferito kaj cementito.
Aliaj mikro-komponantoj[redakti | redakti fonton]

La antaŭaj komponantoj estas haveblaj per malvarmigi la karbonajn ŝtalojn tre malrapide, tamen se oni modifas tiun kondiĉojn (varmotraktado) oni eblas produkti aliajn kristalajn strukturojn[14].:
La martensito estas la komponanto tipa de la harditaj ŝtaloj[13](Tio estas rapidega malvarmigo de ĉirkaŭ 800 °C al ĉambra temperaturo, tio kaŭzas ke la ŝtalo pliduriĝu). Ĝi estas supersaturitaj solvaĵo el karbono kaj α-fero kiu des pli kvanto da karbono emas anstataŭigi la korpocentran kuban strukturon per korpocentra kvar-angula strukturo. Post la cementito kaj aliaj metal-karbidoj, la martensito estas la plej dura komponanto el la ŝtalo.
La interaj rapidecoj de malvarmigo produktas bainiton, ĝi estas tre simila strukturo ol la perlito, ĝi estas formita de pingloj el ferito kaj cementito sed ĝiaj duktileco kaj eltenemeco estas pli granda ol tiuj de la perlito.
Ankaŭ oni eblas produkti aŭteniton per rapida malvarmigado de alojoj kun "gamemaj elementoj (Tiuj elementoj kiuj stabiligas la γ-feron), kiel la nikelo kaj mangano. Ekzemploj de tiaj ŝtaloj estas la rustorezistaj aŭtenitaj ŝtaloj.
Antaŭe oni identigis du aliaj komponantojn, "sorbito" kaj "troostito" kiuj fakte nure estas perlitoj kun tre malgranda inter-lamena distanco, do tiaj nomoj jam ne plu estas uzataj.
Influo de la ĥemiaj elementoj en la ŝtalo[redakti | redakti fonton]

La klasifikoj normigaj de la ŝtaloj kiel la AISI, ASTM kaj UNS, deklaras la minimumajn kaj maksimumajn kvantojn da ĉiu elemento ĥemia en la ŝtalo. La ĥemiaj elementoj estas aldonataj al ŝtalo por plibonigi ĝiajn mekanikajn kaj ĥemiajn ecojn, kiel ekzemple hardeco, ruztorezisteco, mekanika elteno ktp,. La jena estas listo de ĥemiaj elementoj kaj ĝia influo en la ŝtalaj ecoj:[15][16]
- Aluminio: Je 0.008% kaj malpli kvanto, ĝi funkcias kiel senoksidigo por alt-alojataj ŝtaloj.
- Azoto: Oni aldonas ĝin al la ŝtalo por stimuli la kreadon de aŭstenito.
- Boro: En malmulta kvanto (inter 0.001 ĝis 0.006%) ĝi plibonigas la hardadeblecon. Ĝi miksiĝas kun karbono por krei karbidojn tre malmolajn. Ĝi estas aldonata al ŝtaloj kun eta kvanto da alojaj elementoj kiuj estas uzataj en ŝtalaj plugiloj kaj en metal-fadenoj kiujn bezonas alta duktileco kaj surfaca dureco.
- Kobalto: Ĝi durigas la ŝtalon sed malpligrandigas la profundecon de la hardiĝo. La kobalto ankaŭ plibonigas la eltenon kaj durecon je altaj temperaturoj.
- Kromo: Ĝi kreas tre malmolan karbidon kaj donas al ŝtalo tenacecon, durecon, kaj rezistecon je ajna temperaturo. En kvantoj de ĉirkaŭ 13% aŭ pli, la kromo donas al ŝtalo tre bonan ruztorezistecon. Ankaŭ ĝi pligrandigas la profundecon de la hardiĝo per varmo-traktadoj kiel nitrogenado kaj karburado.
- Molibdeno: Ĝi estas tre kutima aldonaĵo de la ŝtalo, ĝi pligrandigas la profundecon de la hardiĝo. En la aŭstenitaj rustorezistaj ŝtaloj la molibdeno plibonigas la rezistancon kontraŭ la korodo.
- Nikelo: Ĝi stabilas la γ-fazon, tiel ĝi permesas ke la aŭstenita strukturo ekzistu je media temperaturo. Ankaŭ la nikelo plibonigas la eltenon kaj rezistecon kontraŭ kolizioj. Ĝi estas uzata kune kun kromo por plibonigi la ruztorezistecon.
- Plumbo: La plumbo ne miksiĝas kun la ŝtalo, oni povas trovi plumbon en la ŝtalo kiel tre etaj globetoj, tio faciligas la forprenadon de metal-defalaĵoj (per tornado, drilado ktp,.). Oni devas uzi ĝin en kvantoj inter 0.15% kaj 0.30%, sed la kvanto de karbono devas esti limigita al kvantoj sub 0.5%, male la hardado kaj la elteno je altaj temperaturoj malpliboniĝas.
- Silicio: Ĝi pligrandigetas la hardadon kaj ankaŭ pligrandigas la rezistecon de la ŝtaloj kun malalta kvanto da karbono.
- Titano: Oni uzas ĝin por stabili kaj senoksidigi la ŝtalon je altaj temperaturoj. La titano emas miksiĝi kun la karbono, do oni ankaŭ uzas ĝin por eviti la formiĝon de feraj karbidoj dum la veldado.
- Vanadio: Ĝi estas bona senoksidigo kaj ĝi miksiĝas kun la karbono por krei karbidon kompleksajn kun la fero, tio donas al la ŝtalo bonan rezistecon je metal-laciĝo.
- Volframo: Ĝi miksiĝas kun la fero kaj formiĝas tre malmolaj kaj stabilaj karbidoj, kiuj donas al ŝtalo tre bonan rezistecon kaj eltenon je tre altaj temperaturoj. Je kvantoj inter 14-18%, ĝi estas la ĉefa elementoj de la rapidaj ŝtaloj per kiuj oni povas triobligi la rapidecon de tranĉado el laborilaj karbonaj ŝtaloj.
Malpuraĵoj en la ŝtalo[redakti | redakti fonton]

Oni nomas malpuraĵojn al tiuj elementoj ĥemiaj, kiuj oni devas eviti aldoni al la ŝtala komponaĵo. Eblas trovi tiajn elementojn en la ŝtaloj kaj gisferoj ĉar kutime ili estas komponantoj de la mineraloj aŭ fueloj. Oni klopodas forigi ilin aŭ malpligrandigi ilian kvanton en la ŝtalo ĉar tiaj elementoj estas malutilaj por la ecoj de la ŝtaloj kaj alojoj. Se ne eblas forigi ilin aŭ ilia forigado estas tre multe kosta, oni povas akcepti ilin ene de la ŝtalo sed en minumumaj kvantoj.
Sulfuro: Proksimuma maksimuma permesata kvanto: 0,04%. La sulfuro miksiĝas kun la fero kaj kreas sulfidon. Ĝi estas malutila ĉar la sulfido kune kun la aŭstenito formas eŭtekton, kies fandopunkto estas tre malalta.
Oni kontrolas la kvanto da sulfuro per aldonado de mangano. La mangano emas miksiĝi kun la sulfuro, kaj tiuj emo estas pli granda ol tiu de la fero, do la fero ne eblos miksiĝi kun la sulfuro kaj krei sulfidon (La mangano kaj la sulfuro kreas MnS, kies fandopunkto estas alta). Oni kalkulas ke la kvanto da mangano devas esti proksimume kvin-foje la kvanto da sulfuro.
Fosforo: Proksimuma maksimuma permesata kvanto: 0,04%. La fosforo estas malutila ĉar kiam ĝi solvas en la ferito, la duktileco malpligrandiĝas, kaj ankaŭ formas FeP (Fosforido el fero). La FeP kune kun la aŭstenito kaj cementito kreas ternaran eŭtekton, kiu estas tre fragila kaj havas fandopunkton relative malalta.
Industrio[redakti | redakti fonton]

Oni konsideris ŝtalindustrion ofte indikilo de ekonomia progreso, pro la kritika rolo ludita de ŝtalo en infrastruktura kaj ĝenerala ekonomia disvolviĝo.[17] En 1980, estis pli ol 500 000 ŝtallaboristoj en Usono. Ĉirkaŭ 2000, la nombro de ŝtallaboristoj estis falinta al 224 000, nome oni perdis pli ol duono.[18]
La ekonomia eksplodo en Ĉinio kaj Barato okazigis amasan pliigon en la stalpeto. Inter 2000 kaj 2005, la tutmonda ŝtalpeto pliiĝis je ĉirkaŭ 6%. Ekde 2000, kelkaj barataj[19] kaj ĉinaj[20] ŝtalfirmaoj etendiĝis por kontentigi la ŝtalpeton, kiel Tata Steel (kiu aĉetis la Grupon Corus en 2007), Baovu kaj Ŝagang. En 2017, tamen, ArcelorMittal estas la plej granda ŝtalproduktanto en la mondo.[21] En 2005, la British Geological Survey asertis, ke Ĉinio estis la pinta ŝtalproduktanto kun ĉirkaŭ unu triono de la tutmonda produkto; Japanio, Rusio kaj Usono sekvis respektive en tiu ordo.[22]
Usona Ŝtalo (angle United States Steel Corporation, ofte konata kiel U.S. Steel, estas ŝtalproduktanto kun ĉefaj produktadinstalaĵoj en Usono, Kanado kaj Mezeŭropo. La firmao estas la 12-a plej granda ŝtalproduktanto de la mondo (2010). En 1991, ĝi estis renomita USX Corporation, sed revenis al la nomo United States Steel Corporation en 2001, ĉar USX-akciuloj prirezignis siajn ŝtalfaradklopodojn post la akiro (1982) de Marathon Oil kaj Texas Gas. Ĝi restas la plej granda produktanto de ŝtalo en Usono, eĉ se ĝi nur produktas iomete pli da ŝtalo ol ĝi faris en 1902. La firmao estis listigita sur la Dow Jones Industrial Average la 1an de aprilo 1901 ĝis la 3an de majo 1991 [23][24][25][26].
La granda produktokapacito de ŝtalo rezultas ankaŭ en grava kvanto de eksendado de karbondioksido esence rilataj al la ĉefa produkt-itinero. En 2021, oni ĉirkaŭkalkulis, ke ĉirkaŭ 7% de la tutmondaj gaselsendoj kun forceja efiko rezultis ela ŝtalindustrio.[27][28] Oni esperas, ke reduktado de tiuj elsendoj devenu el ŝanĝoj en la ĉefa produkt-itinero kiu uzas karbon, pli da reciklado de ŝtalo kaj la aplikado de karbonkaptado kaj stokado de karbonkaptado kaj uzado de tiurilata teknologio.
Je la fino de 2008, la ŝtalindustrio frontis akran malpliigon kio kondukis al multaj fortranĉoj.[29]
Aliaj produktantoj[redakti | redakti fonton]
Ŝtala reciklado[redakti | redakti fonton]

La ŝtalo, kiel ajna metalo, eblas recikliĝi. Je la fina de iliaj utilaj vivo, ĉiuj la aparataĵoj konstruitaj el ŝtalo kiel, maŝinoj, ŝipoj, veturiloj, trajnoj ktp., povas esti malfaritaj, disigante iliajn malsamajn pecojn laŭ materialo kaj tiel oni akiras metal-rubon (Fakte fer-rubo) kiu estas reciklebla. Oni sendas tiun metal-rubon al fandejo por ke ĝi estu re-fandigata. Per ĉi tiu metodo oni enspezas krudan materialon kaj energio kiuj estus uzotaj en la produktado de nova ŝtalo. Oni kalkulas ke 40% de la ŝtal-bezono estas solvitaj el fer-rubo. La reciklado estas farata laŭ striktaj reguloj por eviti dumlaborajn riskojn kaj damaĝon al la natura medio. La personoj kiuj estas en kontakto kun la fer-rubo nepre devas esti vakcinigita kontraŭ la tetanoso, ĉar la ebleco vundiĝi estas alta.
Uzoj[redakti | redakti fonton]

Oni uzas feron kaj ŝtalon amplekse en la konstruado de ŝoseoj, fervojoj, aliaj infrastrukturoj, elektraparatoj, kaj konstruaĵoj. Plimulto de grandaj modernaj strukturoj, kiel stadionoj kaj nuboskrapuloj, pontoj kaj flughavenoj, estas subtenitaj de ŝtala skeleto. Eĉ tiuj kiuj havas betonan strukturon uzas ŝtalon por plifortigo. Oni faras disvastigan uzadon de ŝtalo en grandaj elektraparatoj (nome lavmaŝinoj fridujoj kaj kuirmaŝinoj) kaj aŭtoj. Spite la kreskon en la uzado de aluminio, ŝtalo estas ankoraŭ la ĉefa materialo por aŭtostrukturoj. Ŝtalo estas uzata en vario de aliaj konstrumaterialoj, kiel boltoj, najloj kaj ŝraŭboj kaj aliaj domproduktoj kaj kuiriloj.[30]
Aliaj oftaj aplikaĵoj estas ŝipkonstruado, tubtransportado, minado, markonstruaj instalaĵoj, aerospaco, grandaj elektraparatoj, pezekipaĵaro kiel buldozoj, oficeja meblaro, ŝtal-lano, ilaro, kaj armaĵoj en formo de personaj vestoŝirmiloj aŭ de vehiklarmaĵoj.
Referencoj[redakti | redakti fonton]
- ↑ Oni taskas la kvanto da fero en la tera surfaco kiel 6% [1], dume la lignokarbo estis facile akirebla el la grandaj arbaraj masoj por la fabrikado de ŝtalo. La industriiĝo de la ŝtalproduktado devigis anstataŭigi la lignokarbon per la minkarbo, kies abundeco en la tera surfaco estas taskita je ĉirkaŭ 0,2% [2].
- ↑ 2,0 2,1 pluraj aŭtoroj. (1984) Enciklopedio pri scienco kaj tekniko:1- parto ŝtalo (hispane). ISBN 84-345-4490-3.
- ↑ Civilizations in Africa: The Iron Age South of the Sahara. Arkivita el la originalo je 2011-05-03. Alirita 2013-01-29.
- ↑ Needham, Joseph. (1986) Science and Civilization in China: Volume 4, Part 3, Civil Engineering and Nautics, p. 563.
- ↑ Sanderson Katharine (15-a de novembro 2006). Sharpest cut from nanotube sword: Carbon nanotech may have given swords of Damascus their edge (angle). eldonejo Nature.
- ↑ Robert Hartwell, 'Markets, Technology and the Structure of Enterprise in the Development of the Eleventh Century Chinese Iron and Steel Industry' Journal of Economic History 26 (1966). pp. 53-54
- ↑ Swank, James Moore (1892). History of the Manufacture of Iron in All Ages. Burt Franklin Publisher. ISBN 0-8337-3463-6.
- ↑ Bessemer process. Vol. 2. Encyclopædia Britannica. 2005. p. 168.
- ↑ Metalurgia muzeo el Elgóibar. Arkivita el la originalo je 2007-05-01. Alirita 2013-02-04.
- ↑ Francisko Azorín, arkitekto, Universala Terminologio de la Arkitekturo (arkeologio, arto, konstruo k. metio), Presejo Chulilla y Ángel, Madrido, 1932, paĝo 194.
- ↑ Azorín, samloke.
- ↑ Guy Murry. Fero kaj ĝiaj alojoj: Ŝtaloj, ĝeneralaĵoj (france) 30 paĝoj.
- ↑ 13,0 13,1 13,2 Vetter, Rob. [1988] (1999) Fazodiagramoj (Libro) (esperante), p. 42.
- ↑ J.P. Baïlon, J.M. Dorlot (2000). Des matériaux (Materialoj) (france) p. 1-317, Meĥanikaj proprecoj de materialoj.versio 3-a eldono.
- ↑ Tabulo pri la akcepteblaj procentaĵoj el 8 komponentoj de la normigaj ŝtaloj AISI/SAE. Arkivita el la originalo je 2007-06-10. Alirita 2013-02-08.
- ↑ Publio Galeano Peña. Alojitaj ŝtaloj (hispane). Materiales metálicos. Arkivita el la originalo je 2011-09-10. Alirita 27-a de junio 2011.
- ↑ Steel Industry. Arkivita el la originalo je 2009-06-18. Alirita 2009-07-12.
- ↑ "Congressional Record V. 148, Pt. 4, April 11, 2002 to April 24, 2002". United States Government Printing Office.
- ↑ Chopra, Anuj (12a de Februaro, 2007) India's steel industry steps onto world stage. Cristian Science Monitor. Alirita 2009-07-12.
- ↑ Worldsteel | World crude steel output decreases by -2.8% in 2015. Arkivita el la originalo je 2017-02-02. Alirita 2016-12-26.
- ↑ Top Steelmakers in 2017. World Steel Association. Arkivita el la originalo je 23a de Aŭgusto, 2018. Alirita 22a de Aŭgusto, 2018.
- ↑ Long-term planning needed to meet steel demand. The News (2008-03-01). Arkivita el la originalo je 2010-11-02. Alirita 2010-11-02.
- ↑ United States Steel Corp, X:NYQ profile - FT.com. Alirita 2023-07-05.
- ↑ Hitchcock's Holdup by Sam Tamburro. The Cleveland Memory Project. Alirita 17a de Aprilo 2017.
- ↑ US Steel: first billion-dollar company. Alirita 2023-01-19.
- ↑ United States Steel Corporation History. FundingUniverse. Alirita 3a de Januaro 2014.
- ↑ . The Race to Remake the $2.5 Trillion Steel Industry With Green Steel (en-US) (2022-08-04). Alirita 2022-08-06.
- ↑ Global Steel Industry's GHG Emissions (en-US) (6a de Januaro 2021). Alirita 2022-08-06.
- ↑ Uchitelle, Louis, "Steel Industry, in Slump, Looks to Federal Stimulus", 2009-01-01.
- ↑ “Steel in 20th Century Architecture”, Encyclopedia of Twentieth Century Architecture.
Bibliografio[redakti | redakti fonton]
- Ashby, Michael F.; Jones, David Rayner Hunkin (1992). An introduction to microstructures, processing and design. Butterworth-Heinemann.
- Barraclough, K. C. (1984). Steel before Bessemer: I Blister Steel: the birth of an industry. London: The Metals Society.
- Bugayev, K.; Konovalov, Y.; Bychkov, Y.; Tretyakov, E.; Savin, Ivan V. (2001). Iron and Steel Production. The Minerva Group, Inc. ISBN 978-0-89499-109-7.
- J.C. Carr kaj W. Taplin, History of the British Steel Industry. Harvard University Press, 1962.
- Duncan Burn, The Economic History of Steelmaking, 1867–1939: A Study in Competition. Cambridge University Press, 1961.
- Davidson, H. R. Ellis (1994). The Sword in Anglo-Saxon England: Its Archaeology and Literature. Woodbridge, Suffolk, UK: Boydell Press. ISBN 0-85115-355-0.
- Degarmo, E. Paul; Black, J T.; Kohser, Ronald A. (2003). Materials and Processes in Manufacturing (9a eld.). Wiley. ISBN 0-471-65653-4.
- Fruehan, R. J.; Wakelin, David H. (1998). The Making, Shaping, and Treating of Steel (11a eld.). Pittsburgh, PA: AISE Steel Foundation. ISBN 0-930767-03-9.
- Harukiyu Hasegawa, The Steel Industry in Japan: A Comparison with Britain. Routledge, 1996.
- Mark Reutter, Making Steel: Sparrows Point and the Rise and Ruin of American Industrial Might. University of Illinois Press, 2005.
- H. Lee Scamehorn, Mill & Mine: The Cf&I in the Twentieth Century. University of Nebraska Press, 1992.
- Smith, William F.; Hashemi, Javad (2006). Foundations of Materials Science and Engineering (4a eld.). McGraw-Hill. ISBN 0-07-295358-6.
- Verein Deutscher Eisenhüttenleute (Eld.). Steel – A Handbook for Materials Research and Engineering, Volume 1: Fundamentals. Springer-Verlag Berlin, Heidelberg kaj Verlag Stahleisen, Düsseldorf 1992, 737 p. ISBN 3-540-52968-3, 3-514-00377-7.
- Verein Deutscher Eisenhüttenleute (Eld.). Steel – A Handbook for Materials Research and Engineering, Volume 2: Applications. Springer-Verlag Berlin, Heidelberg kaj Verlag Stahleisen, Düsseldorf 1993, 839 pages, ISBN 3-540-54075-X, 3-514-00378-5.
- Warren, Kenneth, Big Steel: The First Century of the United States Steel Corporation, 1901–2001. University of Pittsburgh Press, 2001.
Vidu ankaŭ[redakti | redakti fonton]
Eksteraj ligiloj[redakti | redakti fonton]
- Oficiala retejo de la World Steel Association (worldsteel)
- steeluniversity.org: Online steel education resources, an initiative of World Steel Association
- Metalurgio por Nemetalurgiistoj el American Society for Metals
- MATDAT Database of Properties of Unalloyed, Low-Alloy and High-Alloy Steels datumbazo pri diversaj alojoj
