Kvaramina kupra (II) sulfato
| Kvaramina kupra (II) sulfato | ||
  . .
| ||
| Kemia strukturo de la Kvaramina kupra (II) sulfato | ||
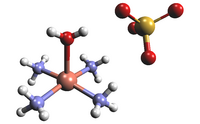
| ||
| 3D Kemia strukturo Kvaramina kupra (II) sulfato | ||

| ||
| Bluaj kristaloj de kvaramina kupra (II) sulfato | ||
| Alternativa(j) nomo(j) | ||
| Kvaramina kuprika sulfato | ||
| Kemia formulo | ||
| CAS-numero-kodo | 14283-05-7 | |
| PubChem-kodo | 61513 | |
| ChemSpider kodo | 430903 | |
| Fizikaj proprecoj | ||
| Aspekto | intense blua kristala solido kun amoniakodoro. | |
| Molmaso | 245,79 g mol−1 | |
| Denseco |
| |
| Bolpunkto | 330 °C (626 ℉; 603 K) | |
| Solvebleco | Akvo:18.5 g/100 g (21.5 °C) | |
| Sekurecaj Indikoj | ||
| Risko | R36/37/38 | |
| Sekureco | S26 S37/39 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS etikedigo de kemiaĵoj[1] | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335, H410 | |
| GHS Deklaroj pri antaŭgardoj | P261, P273, P305+351+338, P391, P501 | |
(25 °C kaj 100 kPa) | ||
Kvaramina kupra (II) sulfato, sulfato de kupro (II) kvaramino aŭ [Cu(NH3)4]SO4.n(H2O) estas neorganika kombinaĵo, malhela blusolido, metala komplekso kun odoro je amoniako. Ĝi intime rilatas al la reakcianto de Schweizer[2], kiu uzatas por produktiĝo de celulozaj fibroj en estiĝo de rajono. Ĝi uzatas por tekstila presado, pesticido kaj en fabrikado de aliaj kupraj kombinaĵoj kiel kupra nano-partikloj.
Sintezo[redakti | redakti fonton]
Amonia kuprika komplekso estas facile preparebla reakciigante akvosolvaĵon de kuprika sulfato kaj amoniako[3].
La profunde blua kristala solido inklinas al hidrolizado kaj liberigo de amoniako kiam ekspoziciita en la aero. Ĝi estas tre solvebla en akvo. La brile malhela blu-viola solvaĵo de kvaramina kupra sulfato havas tian koloron pro la ĉeesto de la katjono [Cu(NH3)4]2+. Ofte, la malhela blu-violkoloro uzatas kiel pozitiva testo por konfirmiĝo de la ĉeesto de katjono Cu2+ en solvaĵo.
Malkomponiĝa reakcio de la kvaramina kuprika sulfato:
Korodo[redakti | redakti fonton]
La karakteriza forte blua koloro de la kvaramina komplekso trovatas en latuno kaj kupraj alojoj kie amoniatako ofte okazas rezultante en molekula krakigo. La problemo unue okazis en ujoj por municiaj kartoĉoj kiuj estis stokitaj apud besto-rubaĵoj, kiuj estigas reziduojn da amoniako. Ĉi-tiu korodotipo konatas kiel sazona krakigo[4].
Uzoj[redakti | redakti fonton]
Plejmulto el la pesticidoj enhavas amonian sulfaton. Kvaramina kupra sulfato ofte uzatas kiel startan materialon por fabrikado de amonia sulfato. Amonia sulfato uzatas kiel aldonaĵo en agrikultura sprajo por akvosolveblaj insekticidoj, herbicidoj kaj fungicidoj. Ĝia ĉefa funkcio estas ligi katjonojn de fero kaj kalcio kiuj ĉeestas, kaj en akvoputoj, kaj en plantoĉeloj. Ĝi estas aparte efektiva kiel aldonaĵo al 2,4-D-amina glifosato kaj herbicidoj surbaze de glufozinatoj. La brile malhela bluviolkoloro kaj ĝia bona solvebleco igas kvaraminan kupran (II) sulfaton bonega kemiaĵo por tekstila tinkturo. Kelkaj el la plej modernaj esploroj kaj eksperimentoj surbaze de kupro inkluvias plurajn studojn pri kvaramina kuprika sulfato. Unu el tiuj esploroj estas la "Kemia reduktiĝo-metodo por preparado de kupra nanopartikloj kun alta pureco uzante natria hipofosfito kiel reduktanto", kiu faras uzon de la kvaramina kupra (II) sulfato.
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- Marked by teachers
- University of Alberta Arkivigite je 2015-09-23 per la retarkivo Wayback Machine
- Laboratory Manual for Principles of General Chemistry, Jo Allan Beran
- Edexcel AS/A2 Chemistry Student Unit Guide: Units 3 and 6 Chemistry ..., George Facer
Belaj prezentaĵoj de Youtube[redakti | redakti fonton]
- Anhidra kvaramina kupra sulfato
- Kvaramina kupra persulfato
- Kvaramina kupra sulfato kaj kupra hidroksido
- Eksperimentoj per kvaramina kupra sulfato
Referencoj[redakti | redakti fonton]
- ↑ Sigma-Aldrich
- ↑ Illustrated Guide to Home Chemistry Experiments: All Lab, No Lecture, Robert Bruce Thompson
- ↑ Make Tetraamminecopper(II) sulfate
- ↑ A Textbook of Engineering Material and Metallurgy, Amandeep Singh Wadhwa, Er. Harvinder Singh Dhaliwal
| ||||||



![{\displaystyle {\mathsf {CuSO_{4}+4\;NH_{3}\cdot H_{2}O\ {\xrightarrow {}}\ [Cu(NH_{3})_{4}]SO_{4}.4H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/224ac7e76830b04a7d1fbf0ea8c8cfb834632694)
![{\displaystyle \mathrm {[Cu(NH_{3})_{4}]^{\,2+}{\xrightarrow {varmo}}\ Cu^{\,2+}+4\ NH_{3}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/87d515d60bcc1b8860e4249c0a9dba2b0bdb6e4c)
