Amonia karbamato
| Amonia karbamato | |||

| |||
| Kemia strukturo de la Amonia karbamato | |||
| Kemia formulo | |||
| CAS-numero-kodo | 1111-78-0 | ||
| ChemSpider kodo | 451267 | ||
| PubChem-kodo | 517232 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkoloraj aŭ blankaj rombaj kristaloj | ||
| Molmaso | 78,0705 g mol−1 | ||
| Denseco | 1.38 (20 °C) g/cm3 | ||
| Fandopunkto | 152 °C (306 ℉; 425 K) | ||
| Bolpunkto | 251 °C (484 ℉; 524 K) ĉe 760 mm Hg | ||
| Solvebleco | |||
| Ekflama temperaturo | 105.6 °C (222.1 ℉; 378.8 K) °C | ||
| Sekurecaj Indikoj | |||
| Risko | R22 R23 R24 R34 R36 R38 | ||
| Sekureco | S3 S20 S24 S25 S43 S60 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H302, H315, H318 | ||
| GHS Deklaroj pri antaŭgardoj | P264, P270, P280, P302, P302+352, P305+351+338, P301+312, P338, P313, P501 | ||
(25 °C kaj 100 kPa) | |||
Amonia karbamato, karbamato de amonio aŭ NH2COONH4 estas neorganika salo de karbamata acido kaj amoniako. Ĉi-komponaĵo estas blanka solido, tre solvebla en akvo kaj etanolo, kaj iomete volatila ĉe meditemperaturo. Ĝi estas senpere estigita pere de reakcio inter la likva amoniako kaj seka glacio.
Sintezo[redakti | redakti fonton]
- Gasamoniako kaj karbona duoksido senpere unuiĝas por estigi amonian karbamaton[1]:
- La reakcio povas okazi en du etapoj[2]:
Reakcioj[redakti | redakti fonton]
Amonia karbamato povas senhidratiĝi al ureo laŭ la jena ekvacio[3]:
Ĝi same povas malkomponiĝi al amoniako kaj karbona duoksido:
Amonia karbamato suferas retroirigan hidratiĝon al amonia karbonato:
Uzoj[redakti | redakti fonton]
La kapableco de la amonia karbamato estigi ureon estis unue malkovrita en 1868[4] de Aleksandro Bazarov (1845-1907)[5], kiam li varmigis en sigelita vitra tubo ĉe temperaturoj variantaj inter 130 °C kaj 140 °C. Ĉi-tio permesis produktadon de ureo kaj akvo egalmolaj kvantoj. Tipa industria instalaĵo por produktado de ureo povas atingi 15000 tunoj potage. Troo da amoniako kaj karbona duoksido devas plenigi reaktoron en ĉi-procezo. Amonia karbamato produktiĝas kiel pera substanco en ĉi-reaktoro kaj povas senhidratiĝi al ureo laŭ la jena ekvacio:
Amonia karbamato aprobiĝas de la "Usona Agentejo por Vivmedia protektado" (EPA[6]) kiel inerta ingredienco ĉeestanta en formuliĝoj por pesticidoj surbaze de "aluminia fosfido". Ĉi-pesticido ordinare uzatas por kontrolo de insektoj kaj roduloj en areoj kie agrikulturaj produktoj enstokiĝas. La kialo por la uzo de la amonia karbamato kiel ingredienco estas igi la fosfinon malpli bruligebla per liberigo de amoniako kaj karbona duoksido por dilui fosfidan acidon estigitan pere de hidroliza reakcio.
Amonia karbamato povas same uziĝi kiel amoniigagento, tamen, kompare kun amoniako, ĝi ne estas tiel forta amoniiganto.
Sintezo de karbamoila fosfato[redakti | redakti fonton]
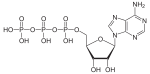
Amonia karbamato plenumas gravan rolon en la formado de "karbamoila fosfato", kiu necesas, kaj por la ciklo de ureo, kaj por la produktado de pirimidinoj. Laŭ ĉi-tiu enzimokataliza reakcio, ATP kaj amonia karbamato konvertiĝas en ADP kaj karbamoila fosfato, tiel kiel en la jena reakcio:
| Sintezo de karbamoila fosfato | ||||||
|

|

|

| |||
| ATP | ||||||
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- The Heat of Formation of Ammonium Carbamate from Ammonia and Carbon Dioxide
- Chemical book
- Snow Engineering: Recent Advances: Proceedings of the third international ..., I. Izumi,T. Nakamura, R.L. Sack
- International critical tables of numerical data, physics, chemistry and ..., Callie Hull
- Yearbook of Pharmacy: Comprising Abstracts of Papers Relating to Pharmacy ..., J. O. Braithwaite
- Yearbook of Pharmacy 1871, John Churchill & Sons
- L.S.A., List of C.F.R. Sections Affected
| ||||||
Referencoj[redakti | redakti fonton]
- ↑ Notes on Qualitative Analysis
- ↑ La uzo de amonia karbamato kiel material kun alte specifa termo-energia denseco. Arkivita el la originalo je 2016-03-05. Alirita 2015-08-06.
- ↑ Industrial & Engineering Chemistry
- ↑ Справочник химика 21
- ↑ Findpatent.ru
- ↑ Usona Agentejo por Vivmedia protektado











