Amonia tiosulfato
| Amonia tiosulfato | |||||

| |||||
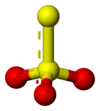
| Kemia strukturo de la amonia tiosulfato | |||||
| |||||
| 3D Kemia strukturo de la amonia tiosulfato | |||||
| Alternativa(j) nomo(j) | |||||
| Duamonia tiosulfato | |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 7783-18-8 | ||||
| ChemSpider kodo | 4807475 | ||||
| PubChem-kodo | 6857883 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkoloraj senodoraj kristaloj | ||||
| Molmaso | 148.20 g mol−1 | ||||
| Smiles | [O-]S([O-])(=O)=S .[NH4+].[NH4+] | ||||
| Denseco |
| ||||
| Fandopunkto | 150 °C (malkomponiĝas) | ||||
| Solvebleco:Akvo | 103.31 g / 100 ml | ||||
| Mortiga dozo (LD50) | 2890 mg kg | ||||
| Sekurecaj Indikoj | |||||
| Risko | R20 R35 | ||||
| Sekureco | S24 S25 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Averto | ||||
| GHS Deklaroj pri damaĝoj | H319 | ||||
| GHS Deklaroj pri antaŭgardoj | P264, P305+351+338, P330, P331[1] | ||||
(25 °C kaj 100 kPa) | |||||
Amonia tiosulfato aŭ (NH4)2S2O3 estas neorganika kombinaĵo, kristalblanka solido kun amoniakodoro, tre facile solvebla en akvo, iom solvebla en acetono kaj nesolvebla en etanolo kaj etero. La salo rezultas el reakcio inter la "tiosulfata acido" kaj amonia hidroksido. Amonia tiosulfato uzatas por ora kaj arĝenta ekstraktado, kiel katalizilo en la ĉeesto de kupro kaj amoniako.
Ĉi-procezo estas alternativa netoksa orcianigo. Ĝi same uzatas kiel sterko. Laŭ kelkaj esploroj antaŭnelonge faritaj, amonia tiosulfato uzatas kiel aldonaĵo al miksaĵoj da karbonrestaĵoj por reduktado de tre danĝeraj dioksinoj kaj furanoj. Amonia tiosulfato uzatas ankaŭ kiel fotografio-fiksanto, pli efika ol la egalvalora natria tiosulfato. La fiksado implicas kelkaj kemiajn reakciojn kun la arĝenta bromido.
Sintezo[redakti | redakti fonton]
Reakcio inter la amonia sulfito kaj sulfuro.
Reakcio inter amoniako, sulfida acido kaj hidrogena peroksido:
Reakcioj[redakti | redakti fonton]
Amonia tiosulfato malkomponiĝas kiam varmigita per estigo da amonia sulfato, amoniako kaj sulfida acido:
En diluitaj solvaĵoj ĝi iompostiom malkomponiĝas en "amonia sulfito" kaj sulfuro:
En diluitaj acido-solvajoj ĝi laŭgrade malkomponiĝas en amonia salo de la acido, sulfura duoksido, sulfuro kaj akvo.
En varmaj kaj koncentritaj acido-solvaĵoj ĝi reakcias per estigo de amonia salo de la acido, sulfata acido kaj sulfida acido.
Amonia tiosulfato reakcias kun halogenidoj kaj akvo:
Literaturo[redakti | redakti fonton]
- American Elements
- Sigma-Aldrich
- Fischer Scientific Arkivigite je 2015-07-22 per la retarkivo Wayback Machine
- Santa Cruz Biotechnology
- CropNutrition
- Gas Purification, Arthur L Kohl, Richard Nielsen
- The Darkroom Cookbook, Steve Anchell
- Hazardous Materials: Emergency Action Data, Charles R. Foden, Jack L. Weddell
- Industrial Inorganic Chemistry, Karl Heinz Büchel, Hans-Heinrich Moretto, Dietmar Werner
- Gardner's Commercially Important Chemicals: Synonyms, Trade Names, and ..., G. W. A. Milne
Referencoj[redakti | redakti fonton]
| ||||||












