Kalia permanganato
| Kalia permanganato | |||||
 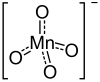 | |||||
| Plata kemia strukturo de la Kalia permanganato | |||||
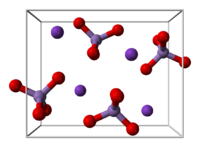 | |||||
| Kristalografa strukturo de la Kalia permanganato | |||||
 | |||||
| Kristaloj de Kalia permanganato | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 7722-64-7 | ||||
| ChemSpider kodo | 22810 | ||||
| PubChem-kodo | 516875 | ||||
| Merck Index | 14,7655 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | purpuro-bronzo-grizaj nadloj, ruĝeco-rozkolora en solvaĵo | ||||
| Molmaso | 158.034 g·mol-1 | ||||
| Denseco | 2.703 g cm−3 | ||||
| Fandpunkto | 240 °C | ||||
| Refrakta indico | 1,5900 | ||||
| Acideco (pKa) | -0.3 | ||||
| Solvebleco | Akvo: | ||||
| Mortiga dozo (LD50) | 1090 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Risko | R8 R22 R34 R36/38 R50/53 R52/53 | ||||
| Sekureco | S26S36S60 S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H272, H302, H314, H410 | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P220, P221, P264, P270, P273, P280, P301, P305+351+338, P310, P330, P391, P501 | ||||
(25 °C kaj 100 kPa) | |||||
Kalia permanganato (KMnO4) estas viola-nigra, iomete metalluma, brileta kristala solidaĵo kaj ĝi solviĝas bone en akvo. La solvaĵo havas la malhelviolan koloron kaj efikon de forta oksidenzo. La kemiaĵo forte oksidigas la organikajn materialojn. Oni uzas ĝin por blankigo de la teksaĵoj, purigo de organikaj matrialoj, „tanado” de ligno. La akva solvaĵo de la kalia permanganto havas sterilizan efikon.
Oni uzas ĝin en la analitika kemio kiel la plej gravan reagenton de la oksidiga titrado.
La silabo per signifas en la kemio, la mangano aperas en la eble plej alta oksidiĝa stato, nome +7.
Produktado[redakti | redakti fonton]
La teknika produktado okazas el brunŝtono MnO2, kiu reagas kun kalia hidroksido kaj aera oksigeno al verdkolora kalia manganato (VI) K2MnO4. Tiu estas elektrokemie plu-prilaborita al kalia permanganato (anoda oksidiĝo) kaj aperas en al komerco la kristala formo.
Historio[redakti | redakti fonton]
La fotografistoj uzis kalian permanganaton kiel eron en fulmila pulvoro.
Vidu ankaŭ[redakti | redakti fonton]
| ||||||









