El Vikipedio, la libera enciklopedio
Kalia pirosulfato
Plata kemia strukturo de la Kalia pirosulfato
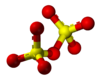
Tridimensia kemia strukturo de la Kalia pirosulfato
Alternativa(j) nomo(j)
Pirosulfato de kalio
Kalia salo de la pirosulfata acido
Dusulfato de kalio
Metabisulfato de kalio
Kemia formulo K2 S2 O7
CAS-numero-kodo 7790-62-7
ChemSpider kodo 56432
PubChem-kodo 62681
Merck Index 15,7784
Fizikaj proprecoj
Aspekto senkolora aŭ blanka solidaĵo
Molmaso 254.3224 g·mol−1
Denseco 2,277g cm−3
Fandpunkto 414 °C [1]
Bolpunkto 600 °C (malkomponiĝas)
Solvebleco Akvo :Tute solvebla
Mortiga dozo (LD50) 2340 mg/kg (buŝe)[2]
Sekurecaj Indikoj
Riskoj R23 R35 [3]
Sekureco S45 S36/37/39 S26
Pridanĝeraj indikoj
Danĝero
GHS Damaĝo Piktogramo
GHS Signalvorto Damaĝa substanco
GHS Deklaroj pri damaĝoj H314 , H318 , H331
GHS Deklaroj pri antaŭgardoj P260 , P261 , P264 , P271 , P280 , P301+330+331 , P303+361+353 , P304+340 , P305+351+338 , P310 , P311 , P321 , P363 , P403+233 , P405 , P501 [4]
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo25 °C kaj 100 kPa)
Kalia pirosulfato , Dusulfato de kalio aŭ K2 S2 O7 estas okso-acido de sulfuro , senkolora aŭ blanka solido rezultanta el varma senhidratigo de la kalia bisulfato . Ĝi estas konata ankaŭ kiel kalia oleumo ĉar ĝia acido estas la ĉefa konstituanto de la fumanta sulfata acido . Pirosulfatoj uzatas en tinkturado, eksplodaĵoj, kaj sintezo de kemiaj kombinaĵoj. En akva solvaĵo ĝi produktas kaliajn katjonojn (K+ )kaj pirosulfatajn anjonojn (S2 O2 −2 ).
2
K
H
S
O
4
→
250
o
C
−
310
o
C
K
2
S
2
O
7
+
H
2
O
{\displaystyle {2\,KHSO_{4}{\xrightarrow[{}]{250^{o}C-310^{o}C}}K_{2}S_{2}O_{7}+H_{2}O}}
2
K
H
S
O
4
+
S
O
3
→
K
2
S
2
O
7
+
H
2
S
O
4
{\displaystyle {2\,KHSO_{4}+SO_{3}{\xrightarrow[{}]{}}K_{2}S_{2}O_{7}+H_{2}SO_{4}}}
2
K
O
H
+
2
S
O
3
→
K
2
S
2
O
7
+
H
2
O
{\displaystyle {2\,KOH+2\,SO_{3}{\xrightarrow[{}]{}}K_{2}S_{2}O_{7}+H_{2}O}}
Pirosulfato de kalia malkomponiĝas kun liberigo de sulfura trioksido kiam temperaturo atingas inter 300 °C kaj 700 °C [6]
K
2
S
2
O
7
→
300
o
C
−
700
o
C
K
2
S
O
4
+
S
O
3
↑
{\displaystyle {\mathsf {K_{2}S_{2}O_{7}\ {\xrightarrow {300^{o}C-700^{o}C}}\ K_{2}SO_{4}+SO_{3}\uparrow }}}
A
l
2
O
3
+
3
K
2
S
2
O
7
→
T
A
l
2
(
S
O
4
)
3
+
3
K
2
S
O
4
{\displaystyle {\mathsf {Al_{2}O_{3}+3\;K_{2}S_{2}O_{7}\ {\xrightarrow {T}}\ Al_{2}(SO_{4})_{3}+3\;K_{2}SO_{4}}}}
Pirosulfato de kalio reakcias kun titana duoksido :
T
i
O
2
+
2
K
2
S
2
O
7
→
T
T
i
(
S
O
4
)
2
+
2
K
2
S
O
4
{\displaystyle {\mathsf {TiO_{2}+2\;K_{2}S_{2}O_{7}\ {\xrightarrow {T}}\ Ti(SO_{4})_{2}+2\;K_{2}SO_{4}}}}
Pirosulfato de kalio reakcias kun metil-hidrazino por doni metil-hidrazino-sulfonato de kalio[7]
K
2
S
2
O
7
+
H
3
C
−
N
H
N
H
2
→
T
H
3
C
−
N
H
N
H
S
O
3
K
m
e
t
i
l
−
h
i
d
r
a
z
i
n
o
−
s
u
l
f
o
n
a
t
o
d
e
k
a
l
i
o
+
K
H
S
O
4
b
i
s
u
l
f
a
t
o
d
e
k
a
l
i
o
{\displaystyle {\mathsf {K_{2}S_{2}O_{7}+H3C-NHNH_{2}\ {\xrightarrow {T}}\ {\underset {metil-hidrazino-sulfonato\,de\,kalio}{H_{3}C-NHNHSO_{3}K}}+{\underset {bisulfato\,de\,kalio}{KHSO_{4}}}}}}
K
2
S
2
O
7
+
2
K
O
H
→
T
K
2
S
O
4
s
u
l
f
a
t
o
d
e
k
a
l
i
o
+
H
2
O
{\displaystyle {\mathsf {K_{2}S_{2}O_{7}+2\,KOH\ {\xrightarrow {T}}\ {\underset {sulfato\,de\,kalio}{K_{2}SO_{4}}}+H_{2}O}}}
Pirosulfato de kalio reakcias kun kromia trioksido donante sulfatojn de kalio kaj kromio (III):
3
K
2
S
2
O
7
+
C
r
2
O
3
→
T
3
K
2
S
O
4
s
u
l
f
a
t
o
d
e
k
a
l
i
o
+
C
r
2
(
S
O
4
)
3
{\displaystyle {\mathsf {3\,K_{2}S_{2}O_{7}+Cr_{2}O_{3}\ {\xrightarrow {T}}\ {\underset {sulfato\,de\,kalio}{3\,K_{2}SO_{4}}}+Cr_{2}(SO_{4})_{3}}}}
Neorganikaj saloj de kalio








![{\displaystyle {2\,KHSO_{4}{\xrightarrow[{}]{250^{o}C-310^{o}C}}K_{2}S_{2}O_{7}+H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ed3d6f45648047dc68e87a0f0fb72313483cb998)
![{\displaystyle {2\,KHSO_{4}+SO_{3}{\xrightarrow[{}]{}}K_{2}S_{2}O_{7}+H_{2}SO_{4}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ab93ac656e7d8286f8d831748e8f944b1a4a2e7c)
![{\displaystyle {2\,KOH+2\,SO_{3}{\xrightarrow[{}]{}}K_{2}S_{2}O_{7}+H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a29a96192cb6785796c0673de9b9fa316e5b736d)






