Kalia stanato
| Kalia stanato (IV) | |||
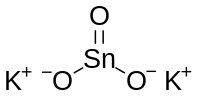 | |||
| Plata kemia strukturo de la Kalia meta-stanato (IV) K2SnO3 | |||
 | |||
| Plata kemia strukturo de la Kalia orto-stanato (VI) K2SnO4 | |||
 | |||
| Tridimensia kemia strukturo de la Kalia meta-stanato (IV) | |||
| Kompleksa formulaĵo de Kalia meta-stanato.3 H2O | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | .3 H2O | ||
| CAS-numero-kodo | 12027-61-1 (anhidra) | ||
| CAS-numero-kodo | (trihidatigita) 12142–33–5 (trihidatigita) | ||
| PubChem-kodo | 61554 | ||
| Merck Index | 15,7791 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ blanka solidaĵo | ||
| Molmaso | 244904 g·mol−1 | ||
| Denseco | 3,197g cm−3[1] | ||
| Fandpunkto | 140 °C (malkomponiĝas) | ||
| Solvebleco | Akvo:reakcias | ||
| Mortiga dozo (LD50) | 178 mg/kg (buŝe)[2] | ||
| Sekurecaj Indikoj | |||
| Riskoj | R34 R36/37/38 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501[3] | ||
(25 °C kaj 100 kPa) | |||
Kalia stanato (IV) aŭ K2SnO3.3 H2O estas neorganika kombinaĵo de kalio, stano kaj oksigeno, senkolora aŭ blanka substanco kun orto-romba kristala strukturo, dum ĝia analogo K4SnO4 estas triklina[4]. Stanatoj troviĝas sub du formoj: metastanatoj prezentantaj la jonon SO3−2 kaj ortostanatoj (IV) aŭ SO4−2.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado de stanato de kalio per traktado de stana (IV) oksido kaj kalia hidroksido[5]:
|
|
Sintezo 2[redakti | redakti fonton]
- Varmigo de orto-stanato de kalio konvertas ĝin sinsekve al K2SnO3, K2Sn3O7 kaj SnO2[6]:
- Malkomponado 1
|
|
- Malkomponado 2
|
|
- Malkomponado 3
|
|
Sintezo 2[redakti | redakti fonton]
- Stanito de kalio reakcias kun bismuta hidroksido por doni kalian stanaton:
|
|
Sintezo 3[redakti | redakti fonton]
- Preparado ekde tri-stanato de kalio kaj kalia hidroksido:
|
|
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Stanato (IV) de kalio reakcias kun akvo:
|
|
Reakcio 2[redakti | redakti fonton]
- Stanato (IV) de kalio reakcias kun fortaj acidoj:
|
|
Reakcio 3[redakti | redakti fonton]
- Stanato de kalio reakcias kun tiostanato de kalio kaj klorida acido:
|
|
Reakcio 4[redakti | redakti fonton]
- Stanato de kalio reakcias kun halogenidoj por doni heksa-stanatojn:
|
|
Reakcio 5[redakti | redakti fonton]
- Stanato de kalio reakcias kun karbona duoksido:
|
|
Reakcio 6[redakti | redakti fonton]
- Stanato de kalio reakcias kun kalcia nitrato:
|
|
Literaturo[redakti | redakti fonton]
- Chemical Book
- American Elements
- Sigma Aldrich
- Alfa Chemistry
- The Complete Technology Book on Electroplating, Phosphating, Powder Coating
- Gardner's Commercially Important Chemicals
Referencoj[redakti | redakti fonton]
| ||||||




![{\displaystyle {SnO_{2}+2\,KOH{\xrightarrow[{precipita{\hat {j}}o}]{blanka}}K_{2}SnO_{3}+H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2faf56f72235fb413f1edffd1e99c6a23909e085)
![{\displaystyle {K_{4}SnO_{4}{\xrightarrow[{}]{varmigo}}{\underset {meta-stanato\,de\,kalio}{K_{2}SnO_{3}}}+K_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c95f776cfa498edf21e07487166dcc0c51090adb)
![{\displaystyle {3\,K_{4}SnO_{4}{\xrightarrow[{}]{900^{o}C}}{\underset {tri-stanato\,de\,kalio}{K_{2}Sn_{3}O_{7}}}+5\,K_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6083f4e49035353e0981577b07b2ae5aec98f53d)
![{\displaystyle {K_{4}SnO_{4}{\xrightarrow[{}]{varmigo}}SnO_{2}+2\,K_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fed35743b6b54a8ee9b6d55098266d82f7a3fe5d)
![{\displaystyle {{\underset {stanito\,de\,kalio}{K_{2}SnO_{2}}}+2\,Bi(OH)_{3}{\xrightarrow[{}]{}}K_{2}SnO_{3}+2\,Bi+3\,H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1934bf6c1c3a0ca102918fdc557b109cbd55fa78)
![{\displaystyle {{\underset {tri-stanato\,de\,kalio}{K_{2}Sn_{3}O_{7}}}+4\,KOH{\xrightarrow[{}]{}}3\,K_{2}SnO_{3}+2\,H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c093b819a8899ded9f7c6c749759ba8d68428de4)
![{\displaystyle {K_{2}SnO_{3}+3H_{2}O{\xrightarrow[{}]{}}{\underset {Heksa-hidrokso-stanato\,de\,kalio}{K_{2}[Sn(OH)_{6}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d5a0cf1ad532f73e69183d713643309a027b39bb)
![{\displaystyle {K_{2}SnO_{3}+6\,HCl{\xrightarrow[{}]{}}2\,KCl+SnCl_{4}+3\,H2O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/864625c4d0d184cc54c55cde51000b729cac60fa)
![{\displaystyle {K_{2}SnO_{3}+2\,K_{2}SnS_{3}+6\,HCl{\xrightarrow[{}]{}}3\,SnS_{2}+6\,KCl+3\,H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/606f4be971580a80517461c483732a8682a17962)
![{\displaystyle {K_{2}SnO_{3}+6\,HI{\xrightarrow[{}]{\ }}{\underset {heksa-jodo-stanato\,de\,kalio}{K_{2}SnI_{6}}}+3\,H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0d58ea5fc438835916ee15007cc0ff7baceb9b5c)
![{\displaystyle {K_{2}SnO_{3}+CO_{2}{\xrightarrow[{}]{}}SnO_{2}+K_{2}CO_{3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9b1a0867bdf698b8e2647cd17f228b9640b918e7)
![{\displaystyle {K_{2}SnO_{3}+Ca(NO_{3})_{2}{\xrightarrow[{}]{}}{\underset {stanato\,de\,kalio}{CaSnO_{3}}}+2\,KNO_{3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3cfdeac221530425c43f0710b369a3f66bcefe5f)
