Natria ferocianido
| Natria ferocianido | ||||
 | ||||
| 3D Kemia strukturo de la Natria ferocianido | ||||
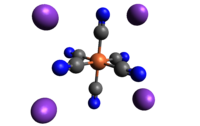 | ||||
| 3D Kemia strukturo de la Natria ferocianido | ||||
 | ||||
| Ebena reprezentado de natria ferocianido | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | Na4Fe(CN)6
| |||
| CAS-numero-kodo | 13601-19-9 | |||
| ChemSpider kodo | 19957180 | |||
| PubChem-kodo | 26129 | |||
| Fizikaj proprecoj | ||||
| Aspekto | palflava kristaloj, senodoraj | |||
| Molmaso |
| |||
| Smiles | [C-]#N.[C-]#N.[C-]#N.[C-]#N.[C-]#N.[C-]#N.[Na+].[Na+].[Na+].[Na+].[Fe+2] | |||
| Denseco | 1,458 g/cm3 | |||
| Refrakta indico | 1,53 | |||
| Fandopunkto | ||||
| Solvebleco: Akvo | ||||
| Nutro-aldonaĵo | E535 | |||
| Mortiga dozo (LD50) | 6400 mg/kg (muso, buŝa) | |||
| Ekflama temperaturo | Ne bruliva | |||
| Sekurecaj Indikoj | ||||
| Risko | R32 R52 R53 | |||
| Sekureco | S22 S24 S25 S50 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS etikedigo de kemiaĵoj[2] | ||||
| GHS Damaĝo-piktogramo | ||||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H300, H302, H310, H312, H330, H400, H410, H412 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P262, P264, P270, P273, P280, P284, P301+312, P302+352, P304+340, P310, P312, P320, P321, P330, P361, P373, P391, P403+233, P405, P501 | |||
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo
(25 °C kaj 100 kPa) | ||||
Natria ferocianido, ferocianido de natrio aŭ Na4Fe(CN)6 estas neorganika natria salo de heksacianata acido aŭ H4[Fe(CN)6]. Ĝi estas flava kristala solido, solvebla en akvo kaj nesolvebla en alkoholo. Malgraŭ la cianidaj (CN) ligantoj[3], natria ferocianido havas malaltan toksecon (taga akceptebla ingestado inter 0 kaj 0,025 mg/kg da korpopezo).
La ferocianidoj estas malpli toksaj ol multaj saloj de cianido, pro tio ke la molekulo inklinas al neliberigo de cianidaj jonoj. Tamen, kiel ĉiuj solvaĵoj de ferocianidaj saloj, aldono de acido povas rezulti en produktado de cianida gaso, kiu estas toksa. Laŭ ĝia dekahidrata formo, Na4Fe(CN)6, estas konata kiel flava prusiato de natrio. La flava koloro apartenas al la anjono ferocianido.
Sintezo[redakti | redakti fonton]
- Reakcio inter fera (II) klorido kaj natria cianido:
- Reakcio inter fera (III) sulfato kaj natria cianido[4]:
- Reakcio inter fera (II) cianido kaj natria cianido:
Reakcio[redakti | redakti fonton]
- Flavo de prusio reakcias kun Fe3+ jonoj por estigi bluon de Prusio[4] :
3 Na4[Fe(CN)6] (Flavo de Prusio) + 4 FeCl3 →
Fe4[Fe(CN)6]3 (Bluo de Prusio) + 12 NaCl}
Fe4[Fe(CN)6]3 (Bluo de Prusio) + 12 NaCl}
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- TheGoodScentsCompany
- United States Environmental Protection Agency
- Toxnet
- Guidelines for the Selection of Snow and Ice Control Materials to Mitigate ..., Levelton Consultants Limited
- A Laboratory History of Chemical Warfare Agents, Jared Ledgard
- The Peaceful Pill Handbook, Philip Nitschke, Fiona Stewart
| ||||||
Referencoj[redakti | redakti fonton]
- ↑ Healthy Bliss
- ↑ PubChem
- ↑ En kemio, liganto estas ĉiu jono aŭ molekulo kiu ligiĝas al la centra metalatomo por estigi kunordigan kompleksaĵon.
- ↑ 4,0 4,1 Cyanide in Water and Soil: Chemistry, Risk, and Management, David A. Dzombak, Rajat S. Ghosh, George M. Wong-Chong








![{\displaystyle {\mathsf {FeCl_{2}+6\;NaCN\ {\xrightarrow {}}\ Na_{4}[Fe(CN)_{6}]+2\;NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/87d2c0e1c923617e6e38f8a30ca9f27ec9b8e2ce)
![{\displaystyle {\mathsf {FeSO_{4}+6\;NaCN\ {\xrightarrow {varmo}}\ Na_{4}[Fe(CN)_{6}]+2\;Na_{2}SO_{4}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c1719717cc5e736d4725e2e740ff0e9a98093a77)
![{\displaystyle {\mathsf {Fe(CN)_{2}+4\;NaCN\ {\xrightarrow {}}\ Na_{4}[Fe(CN)_{6}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a8e2051e84182c401133367ca3a1ea88dcc09455)
