Natria glikolato
Aspekto
| Natria glikolato | |||

| |||
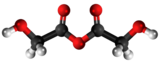
| Kemia strukturo de la Natria glikolato | |||
 | |||
| Tridimensia kemia strukturo de la Kalia glikolato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 2836-32-0 | ||
| ChemSpider kodo | 16840 | ||
| PubChem-kodo | 517347 | ||
| Fizikaj proprecoj | |||
| Aspekto | Blankaj ĝis malhelaj senodoraj kristaloj | ||
| Molmaso | 98,03 g mol−1 | ||
| Smiles | C(C(=O)[O-])O.[Na+] | ||
| Denseco | 1,42 g/cm3 | ||
| Refrakta indico | 1,45 | ||
| Fandopunkto | 210-218 °C | ||
| Bolpunkto | 265.6 °C | ||
| Solvebleco | Akvo:Solvebla | ||
| Mortiga dozo (LD50) | 6700 mg/kg (muso, buŝa) | ||
| Ekflama temperaturo | 128.70 | ||
| Nutro-aldonaĵo | E466 (karboksi-metila glikolato)[1] | ||
| Sekurecaj Indikoj | |||
| Risko | R36/37/38 | ||
| Sekureco | S24/25 S26 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[2] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H315, H318, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P310, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Natria glikolato, glikolato de natrio aŭ OH-CH2-COO-Na estas organika komponaĵo rezultanta el reakcio inter glikolata acido kaj natria hidroksido[3]. En akva solvaĵo natria glikolato suferas hidrolizon estigante glikolatan acidon kaj natrian hidroksidon. La glikolata acido estas acetata acido kun hidroksilo en la dua karbonatomo.
Ĝi same nomatas beta-hidroksiacido. Glikolatoj estas saloj de glikolata acido kaj posedas duoblan funkciecon de alkoholo kaj acido. Pro ĝia eta molekula pezo kaj grando, ĝi facile penetras en la haŭton. Glikolatoj uzatas en kosmetikaĵoj, farmaciaĵoj, nutro-aldonaĵo kiel humidiganto, gustigagento kaj konservaĵo. Natria glikolato estas peranto en organikaj sintezon en oksidaj-reduktaj reakcioj.
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Preparado de natria glikolato per traktado de glikolata acido kun natria hidroksido:
Reakcio 2
[redakti | redakti fonton]- Preparado de natria glikolato per traktado de glikolata anhidrido kun natria hidroksido:
Reakcio 3
[redakti | redakti fonton]- Preparado de natria glikolato per traktado de glikolata acido kun natria klorido:
Reakcio 4
[redakti | redakti fonton]- Preparado de natria glikolato per traktado de glikolata anhidrido kun natria klorido:
Reakcio
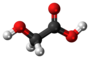
[redakti | redakti fonton]- En akva solvaĵo natria glikolato estigas glikolatan acidon kaj natrian hidroksidon:
Vidu ankaŭ
[redakti | redakti fonton]Literaturo
[redakti | redakti fonton]- ChemicalLand21[rompita ligilo]
- Drugs.com
- LiveStrong
- Chemical Book
- Compendium of Food Additive Specifications: Addendum 10, Edição 52, Food and Agriculture Organization of the United Nations
- Glycolic Acid Peels, Ronald Moy,Debra Luftman,Lenore S. Kakita
| ||||||
Referencoj
[redakti | redakti fonton]- ↑ Codex alimentarius. Arkivita el la originalo je 2015-09-23. Alirita 2015-09-07 .
- ↑ PubChem
- ↑ Cellulose and Cellulose Derivatives in the Food Industry: Fundamentals and ..., Tanja Wuestenberg






![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)