Natria pikrato
| Natria pikrato | |||

| |||
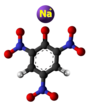
| Kemia strukturo de la Natria pikrato | |||

| |||
| 3D Kemia strukturo de la Natria pikrato | |||
| Alternativa(j) nomo(j) | |||
| Natria salo de pikrata acido | |||
| Kemia formulo | |||
| Aspekto | Flavaj kristaloj | ||
| CAS-numero-kodo | 73771-13-8 | ||
| ChemSpider kodo | 56275 | ||
| PubChem-kodo | 3056390 | ||
| Fizikaj proprecoj | |||
| Molmaso |
| ||
| Bolpunkto | 303.6 °C | ||
| Ekflama temperaturo | 133,9 °C | ||
| Sekurecaj Indikoj | |||
| Risko | R1 R3 R23/24/25 | ||
| Sekureco | (S1/2) S28 S35 S37 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H201, H301, H311, H331 | ||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P261, P264, P270, P271, P280, P281, P301+310, P302+352, P304+340, P311, P312, P321, P330, P361, P363, P372, P373, P380, P401, P403, P233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Natria pikrato, pikrato de natrio aŭ C6H2N3NaO7 estas organika komponaĵo rezultanta el reakcio inter la pikrata acido kaj natria hidroksido aŭ natria bikarbonato. Papero de natria pikrato uzatas en biologio por la kreatinina testo. Ĉeesto de kreatinino en la sango, kiu estas rezulto de la muskolaj klopodoj, indikas ian renmalordon. La testo estas konata kiel testo de Jaffe.[1]
En la reakcio, la kreatinino ligiĝas al la pikrata jono en alkalla medio por krei oranĝo-koloron. La koloro produktita en la specimeno tiam kompariĝas, en kolorimetro kun ondolondo de 505 nm, kun tiu produktita de konata kvanto da kreatinino sub samaj kondiĉoj.[2]
Sintezo[redakti | redakti fonton]
- Neŭtraliga reakcio de pikrata acido kaj natria hidroksido kun estigo de akvo:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Estigo de natria pikramato ekde natria pikrato kaj fera (II) hidroksido kun estigo de akvo kaj fera (III) oksido:
Reakcio 2[redakti | redakti fonton]
- Preparado de natria pikramato ekde natria pikrato kaj natria sulfido en akva medio kun formado de natria tiosulfato kaj natria hidroksido:
Literaturo[redakti | redakti fonton]
- The influence of the color from the sodium picrate in the determination of creatinine in blood and urine
- Reaction of alkaline sodium picrate with creatinine
- Powerlabs Potassium Picrate Synthesis
- Purification of Laboratory Chemicals, W. L. F. Armarego, Christina Li Lin Chai
- The Preparatory Manual of Explosives, Jared Ledgard
- Hands-On Chemical Ecology:: Simple Field and Laboratory Exercises, Dietland Müller-Schwarze
- Plant Secondary Metabolism, David S. Seigle
Youtube[redakti | redakti fonton]
- Metal Picrates - Properties and Mixtures
- Lead picrate
- Potassium Picrate synthesis- Burn Testing
- Lead picrate/Lead azide Clathrate compound
- 30g Ammonal and Lead Picrate
| ||||||
Referencoj[redakti | redakti fonton]
- ↑ Idaho State University[rompita ligilo]
- ↑ International Atomic Energy Agency. Arkivita el la originalo je 2015-09-16. Alirita 2015-10-07.







![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)