Natria trikloroacetato
| Natria trikloroetanato | ||||
| ||||
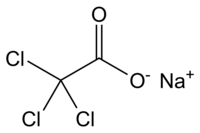
| Kemia strukturo de la Natria trikloroacetato | ||||

| ||||
| 3D Kemia strukturo de la Natria trikloroacetato | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 650-51-1 | |||
| ChemSpider kodo | 12073 | |||
| PubChem-kodo | 23681045 | |||
| Fizikaj proprecoj | ||||
| Aspekto | Senkolora higroskopa solido | |||
| Molmaso | 185,368969 g mol−1 | |||
| Smiles | C(=O)(C(Cl)(Cl)Cl)[O-].[Na+] | |||
| Denseco | 0,9 g/cm3 | |||
| Fandopunkto | 165 °C (malkomponiĝas) | |||
| Solvebleco | Akvo:120 g/100ml | |||
| Nesolvebleco | ||||
| Mortiga dozo (LD50) | 3320 mg/kg (muso, buŝa) | |||
| Ekflama temperaturo | 140 °C °C | |||
| Merck Index | 9627 | |||
| Sekurecaj Indikoj | ||||
| Risko | R37 R50/53 | |||
| Sekureco | S46 S60 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS etikedigo de kemiaĵoj | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Averto | |||
| GHS Deklaroj pri damaĝoj | H301, H315, H319, H351 | |||
| GHS Deklaroj pri antaŭgardoj | P261, P271, P281, P304+340, P312, P305+351+338, P405, P403+233, P501 | |||
(25 °C kaj 100 kPa) | ||||
Natria trikloroacetato, trikloroacetato de natrio aŭ Cl3C-COO-Na estas organika komponaĵo, senkolora kaj higroskopa salo de natria hidroksido kaj trikloroacetata acido, ĉefe uzata kiel oksidanto, fungicido[1], herbicido[2] kaj antimikroba agento. Teknikaj gradoj de la salo estas iom flavecaj. Plejmulto el komercaj preparaĵoj de natria trikloroacetato enhavas 90% de la substanco.
Trikloroaceto de natrio estas irita al okuloj kaj haŭto. Malpurigaĵoj de natria trikloroacetato devas foriĝi per abundo da akvo. Specialaj zorgoj devas preniĝi dum sprajado de trikloroacetato for de ornamentaj plantoj ĉar ĝi povas kaŭzi seriozajn damaĝojn.
Proprecoj[redakti | redakti fonton]
Natria trikloroacetato estis unue enkondukita kiel herbicido en 1947 far E. I. du Pont de Nemours kaj Kompanio, kaj de kompanio Dow Chemical. La buŝdozoj konsiderataj danĝeraj por homuzo estas 3320/kg en ratoj, 4000 mg/kg en kunikloj kaj 4970 en musoj (Woodward, 1941).
Longedaŭraj kontaktoj kun haŭto povas rezulti en kemia brulvundoj kaj la pulvoro de ĉi-substanco estas tre irita al nazo kaj gorĝo. Natria trikloroacetato povas kaŭzi kanceron en homojn. La trikloroacetata acido rezultanta el akvaj solvaĵoj de natria trikloroaceto estas forta acido kun (pKa) ĉirkaŭ 4,75.
Sintezo[redakti | redakti fonton]
- Kompleta neŭtraligo de trikloroacetata acido kaj natria hidroksido:
Literaturo[redakti | redakti fonton]
- Sigma Aldrich
- Molbase
- International Labour Organization
- Chemical Book Arkivigite je 2016-03-05 per la retarkivo Wayback Machine
- Macroscale and Microscale Organic Experiments, Kenneth Williamson, Katherine Masters
- Practical Heterocyclic Chemistry, A. O. Fitton, R. K. Smalley
- The Handbook of Feedstuffs: Production Formulation Medication, Rudolph Seiden, W. H. Pfander
- Chembase Arkivigite je 2016-03-05 per la retarkivo Wayback Machine
Vidu ankaŭ[redakti | redakti fonton]
| ||||||
Referencoj[redakti | redakti fonton]
- ↑ The Pesticide Encyclopedia, Kalyani Paranjape, Vasant Gowariker, V N Krishnamurthy, Sugha Gowariker
- ↑ New Scientist[rompita ligilo]









